נכון לסיום המסחר ב-8 בינואר, מניית בונוס ביוגרופ משלימה זינוק של למעלה מ-60% מאז תחילת 2026, במחזורים גבוהים – וזאת בלי שהחברה פרסמה בתקופה האחרונה עדכונים דרמטיים. בין העדכונים האחרונים ניתן למנות גיוס הון בהיקף שאינו גדול במיוחד (אך בפרמיה למחיר השוק, כפי שהחברה נוהגת לבצע כבר למעלה מעשור), וכן את הודעת הבורסה לניירות ערך בתל אביב על הכללת החברה "במועדון המאה" בדירוג של ארבעה כוכבים, לאחר תשואה למשקיעים בשיעור של מעל 100% בשנת 2025, ובהמשך לתשואה חיובית מצטברת בשלוש השנים האחרונות.
עיון ברשימת "מועדון המאה" מלמד כי בונוס היא חברת הביוטכנולוגיה הישראלית היחידה שנכללת בה, ואחת משתי חברות מו״פ בלבד מכלל הסקטורים שנכנסו לרשימה, נתון שמבליט אותה על רקע האתגרים שחוו חברות מו"פ בשנים האחרונות, ובמיוחד בתחום הביוטכנולוגיה. מעבר לכך, החברה שומרת על "דממת אלחוט" יחסית מאז הדיווח בסוף נובמבר האחרון על הגשת טיוטה פומבית מעודכנת ל-SEC לקראת הנפקה אפשרית בנאסד״ק.
"שעת השין" – תחילת ניסויים קליניים שלב 3
לאחר למעלה מ-13 שנות מו״פ בשני מוצרי הדגל שלה, בונוס ביוגרופ, שנחשבת לחברת ביוטכנולוגיה חריגה בנוף התל-אביבי, נמצאת לקראת אבני דרך משמעותיות. לפי החברה, שני המוצרים שהחברה מפתחת צפויים להתחיל בשלב 3 של ניסויים קליניים, לאחר שהציגו תוצאות חיוביות והצלחות מובהקות בשלב 2.
בונופיל - BonoFill
בונופיל, מוצר הדגל הראשון של החברה, הוא שתל חי של עצם אנושית, המיוצר באמצעות הנדסת רקמות מתאים שמקורם בדגימת שומן של המטופל עצמו, ומיועד לשחזור עצם כחלופה לניתוחי השתלת עצם עצמיים מורכבים.
יתרון חשוב של המוצר הוא שהוא מבוסס על תאי המטופל עצמו, כך שאין חשש לדחייה חיסונית. בנוסף, טיפול באמצעות בונופיל מיועד לחסוך את הצורך בניתוח נוסף לכריתת עצם לצורך שתלת עצם עצמית, פרוצדורה הכרוכה לעיתים בסיבוכים, בעלויות גבוהות ובהחלמה ממושכת.
לפי החברה, פוטנציאל השוק השנתי של בונופיל נאמד במיליוני פרוצדורות ובהיקף של כ-25 מיליארד דולר בשנה (בארה״ב בלבד), וזאת רק בהתוויות של כירורגיית פה ולסת ואורתופדיה הנבדקות כיום בניסויים קליניים. בהמשך, החברה עשויה לפעול להרחבת השימוש במוצר זה גם להתוויות נוספות הקשורות בחוסרים או בפגיעות בעצם.
בניסוי קליני שלב 2 לטיפול בחסרי עצם בפנים (הרמת סינוס ומילוי חללים בלסתות) ביצעה החברה 30 השתלות, ובתום תקופת מעקב של שישה חודשים דווח על שיעור הצלחה מרשים של 90% מהמטופלים בהם נבנתה עצם באזור החסר. כבר לאחר שלושה חודשים מההשתלה, נצפה שיקום מלא של העצם ב-87% מההשתלות, נתון שעשוי להעיד על קיצור משמעותי בזמן ההחלמה.
במקביל, החברה מקדמת ניסוי קליני שלב 2 נוסף לטיפול בחסרי עצם בגפיים, (לרבות איחוי מפרקים ראשון מסוגו בעולם באמצעות שתל עצם מהונדס) המתבצע במספר מרכזים רפואיים בישראל. הניסוי צפוי לכלול עד 40 מטופלים, עד כה טופלו 24 מטופלים, ומדוגמאות קליניות שדווחו על ידי החברה, עולה כי המוצר מציג פרופיל בטיחותי לצד סימני יעילות. עם זאת, החברה טרם פרסמה תוצאות רשמיות מלאות לניסוי זה, ומציינת כי סיום גיוס המטופלים צפוי במהלך 2026.
2 צפייה בגלריה
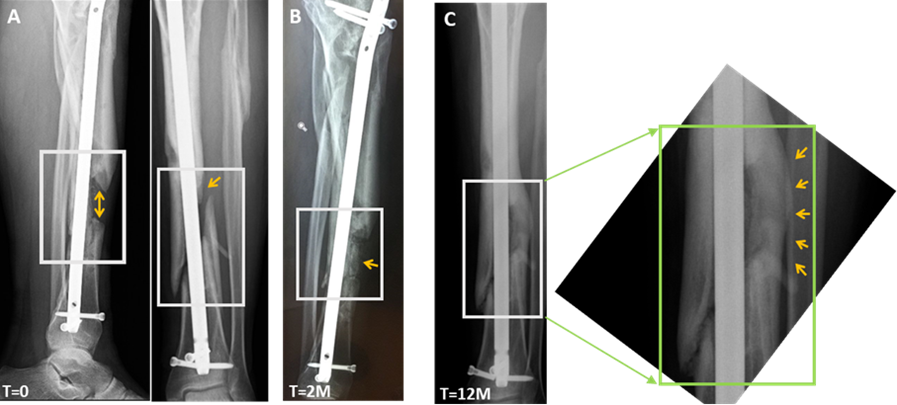

צילומי רנטגן של מטופל שהשתתף במחקר הקליני לטיפול בחסרי עצם בגפיים
(קרדיט: מתוך הדוחות הכספיים של החברה)
צילומי רנטגן של מטופל שהשתתף במחקר הקליני לטיפול בחסרי עצם בגפיים, שסבל מחסר עצם קריטי בגודל של 5 ס"מ בשוק השמאלי ואי יכולת נשיאת משקל. המטופל התלונן על כאב קבוע והיה זקוק לסיוע של קביים כדי ללכת. מצבו היה קשה, ואף נבחנה קטיעה של הגפה. זמן קצר לאחר השתלת בונופיל החולה יכול היה לעמוד על רגלו הפגועה, ללכת ללא עזרה, ואף לקפוץ, תוך כדי ירידה ניכרת בתחושת הכאב. צילומי רנטגן שצולמו לפני הטיפול ([A], T=0) וחודשיים ([B], T=2M), ו-12 חודשים לאחר הטיפול ([C], T=12M) מראים ריפוי מהיר ואיחוי של חסר העצם. אזור החסר מודגש בירוק.
במהלך 2026, החברה מתכננת להתחיל בארה״ב ניסוי קליני שלב 3 לטיפול בחסרי עצם בלסתות, שצפוי לכלול כ-50 מטופלים.
מזנקיור - MesenCure
מזנקיור, המוצר השני של החברה, הוא תרופה המבוססת על תאים חיים לטיפול בדלקות ובנזק לרקמות, כאשר ההתוויה הניסיונית הראשונה היא טיפול בתסמונת מצוקה נשימתית חריפה. במחקר פאזה 2 הודגמה, לפי דיווחי החברה, הפחתה משמעותית של כ-68% בתמותה בקרב 50 חולים קשים עם מצוקה נשימתית על רקע דלקת ריאות מקורונה שטופלו באמצעות מזנקיור, בהשוואה לקבוצת ביקורת של 150 חולים. בנוסף דווחה ירידה של כ-57% בצורך בהנשמה פולשנית, וכן קיצור משך האשפוז של חולים מורכבים בכ-9.4 ימים בממוצע.
תסמונת מצוקה נשימתית חריפה אחראית לכ-10%–15% מתפוסת המיטות ביחידות טיפול נמרץ, ומובילה כיום לתמותה בשיעור של כ-27%–45% מהמקרים. הטיפול המקובל במצב זה כיום אינו מיועד לרפא את המחלה, והוא בעיקר תומך וסימפטומטי, לרבות תמיכה נשימתית וטיפול תרופתי שמטרתו להקל על התסמינים ולייצב את החולה. לפי ממצאי החברה, מזנקיור עשוי להוות טיפול בעל פוטנציאל מציל חיים, ובמקביל להפחית עומס כלכלי באמצעות צמצום ימי אשפוז יקרים למערכת הבריאות.
על רקע מאות אלפי מקרים בארה״ב מדי שנה, גודל השוק הפוטנציאלי של מזנקיור בהתוויה זו מוערך בכ-9.4 מיליארד דולר עד שנת 2030.
2 צפייה בגלריה
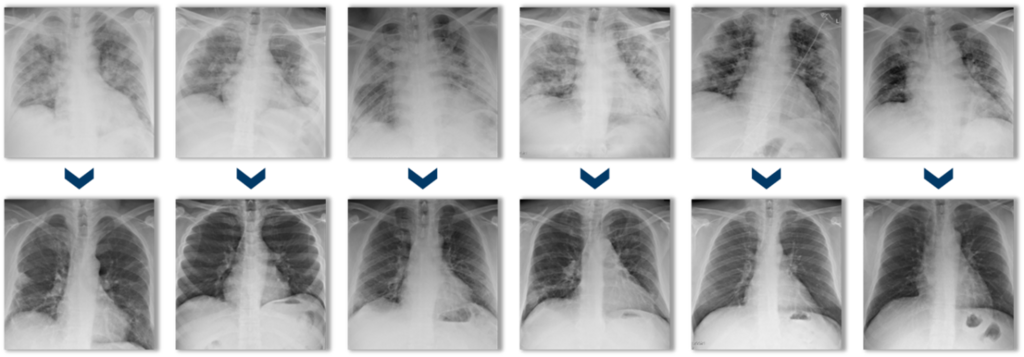

צילומי חזה של שישה מטופלים לפני טיפול במזנקיור (שורה עליונה) וכ-30 יום לאחר מכן (שורה תחתונה)
(קרדיט: מתוך הדוחות הכספיים של החברה)
צילומי חזה של שישה מטופלים לפני טיפול במזנקיור (שורה עליונה) וכ-30 יום לאחר מכן (שורה תחתונה). לפני הטיפול, ריאותיהם של החולים עמוסות בתסנינים דלקתיים (עודף נוזלים, תאי חיסון וחלבונים) החוסמים נשימה תקינה. לאחר הטיפול, הדלקת מתנקה.
הטיפול במזנקיור נעשה באמצעות עירוי לווריד של תאים שמקורם בתורם בריא, אשר עוברים תהליך פטנטי של "אימון" שנועד לחזק את יכולתם להפחית דלקת ולעודד התחדשות רקמה. בדומה לבונופיל, שמיועד לטיפול בחסר עצם ללא קשר למקור החסר, גם התרופה מזנקיור מיועדת לטיפול במצבי דלקת – לרבות דלקת ריאות ותסמונת מצוקה נשימתית – ללא תלות בגורם שהוביל להתפתחותה.
החברה מתכננת להתחיל במהלך 2026 ניסוי קליני בארה״ב לטיפול בחולים קשים עם תסמונת מצוקה נשימתית חריפה מכל סיבה, באמצעות מזנקיור, בהיקף של כ-450 מטופלים.
עם הפנים לנאסד״ק
בונוס ביוגרופ מקדמת רישום והנפקה בנאסד״ק, בהובלת החתם ובנק ההשקעות Titan Partners Group, המתמקד בחברות צמיחה, עם התמחות בתחומי הביוטק והטכנולוגיה.
להערכת החברה, שוק ההון האמריקאי מעניק לסקטור הביוטכנולוגיה חשיפה גבוהה משמעותית בהשוואה לשוק הישראלי, עם מספר גדול בהרבה של חברות בתחום, סיקור אנליטי רחב יותר והשתתפות משמעותית יותר של משקיעים מוסדיים. בהתאם, החברה סבורה כי מהלך כזה עשוי להגדיל את החשיפה הגלובלית שלה, להרחיב את בסיס המשקיעים ולשפר את נגישותה להון. עיקר התמורה מההנפקה מיועדת למימון ניסויים קליניים בפאזה 3 עבור שני מוצרי הדגל של החברה, המוערכים בעלות של כמה עשרות מיליוני דולרים.
ההכנות של החברה לקראת ההנפקה בארה״ב, לצד היערכותה לפתיחת ניסויי שלב 3, עומדות ככל הנראה מאחורי ההתעוררות במניה במחזורים גבוהים. חלק מהמשקיעים מעריכים כי מהלך כזה עשוי להביא לתמחור גבוה יותר מזה שבת״א, על רקע רמות שווי גבוהות יותר של חברות ביוטכנולוגיה הנסחרות בארה״ב, לרבות חברות המצויות בשלבים שונים של פיתוחים דומים.
כך למשל, Capricor Therapeutics (NASDAQ: CAPR) מפתחת טיפול תאי למחלת יתום (דושן) ונמצאת כיום בשלהי ניסוי שלב 3, עם שווי שוק של כ-1.2 מיליארד דולר; וכן Mesoblast (NASDAQ: MESO), חברה בתחום הטיפול התאי שביססה מוצר בעל קווי דמיון רעיוניים לעולם של מזנקיור (גם אם בטכנולוגיה מוקדמת יותר ובהתוויות שונות), אשר השיקה ב-28 במרץ 2025 מוצר מסחרי, גם הוא למחלת יתום, עם שווי שוק של כ-2.5 מיליארד דולר.
סיכויים וסיכונים
לצד האופטימיות העולה ממצגות שהחברה פרסמה לקראת תחילת ניסוי שלב 3 במוצרי הדגל קיים כמובן סיכון שהדברים פחות יצליחו בשלב 3 הנחשב לגדול ומקיף יותר כמו גם כישלון אפשרי של ההנפקה בארה״ב שעשוי להקשות על החברה שעד היום גייסה בכל פעם מיליוני שקלים בודדים בעיקר ממשקיעים פרטיים (לזכותה יאמר שכל ההנפקות מיום הפיכתה לציבורית היו בפרמיה על מחיר השוק ונעשו בהנפקות פרטיות חסומות שלא לחצו את המניה).
באירועים בינאריים של יצליח/לא יצליח התוצאה כמובן עשויה להיות חדה לפה או לשם גם במחיר המניה כך שמדובר בהחלט בהשקעה בסיכון גבוה מאוד לצד הסיכוי. נותר לאחל הצלחה עבור מטופלים רבים שעשויים להנות מאיכות חיים טובה יותר במידה והניסויים יצליחו ויעברו למסחור עם כיסוי ביטוחי למטופלים.
*אין בנכתב המלצה או תחליף ליעוץ.
פרי אמסלם הינו מנהל פלטפורמת בורסה 360 ומשמש כיועץ שוק ההון לחברות ציבוריות ופרטיות. אין לראות באמור המלצה לפעילות בשוק ההון וני״ע השונים. לתכנים נוספים על שוק הישראלי מוזמנים להצטרף לעקוב אחרינו בערוץ הוואטסאפ וכן להצטרף לערוץ הטלגרם
אין לחברת ידיעות תקשורת בע״מ, לאתר ynet או לחברת המברקה פתרונות תקשורת בע״מ זיקה כלשהי לתוכן במובן של ניגוד עניינים או של עניין מיוחד. הכתוב אינו מהווה ייעוץ השקעות ו/או תחליף לייעוץ המתחשב בנתונים ובצרכים המיוחדים של כל אדם. אין לראות במידע בסקירה זו כעובדתי או כמכלול כל המידע הידוע, ולכן אין להסתמך על הכתוב בה ככזה.
פורסם לראשונה: 07:07, 09.01.26





