במקום ניתוח לב פתוח: החידושים בתחום רפואת הלב
תומכן מתכלה לפתיחת חסימות והיצרויות, מסתם זעיר המווסת את מעבר הדם בין העליות בחולי אי ספיקת לב, טלאי לבבי המשלב חלקיקי זהב והשתלת תאי גזע בשריר הלב. אלה הם רק חלק מהחידושים המבטיחים בתחום הקרדיולוגיה בעשור האחרון
איך השתנה הטיפול במחלות לב בעשור האחרון? אם מטופל הסובל מהתקף לב מוכנס לחדר הצנתורים בתוך 90 דקות מהרגע שהגיע לבית החולים, סיכוייו לשרוד גבוהים מאוד וייחסכו ממנו סיבוכים בתהליך ההחלמה. זו הייתה ההסכמה המקובלת בקרב מומחים לקרדיולוגיה בעשורים האחרונים. תפיסה זו אף תורגמה למנטרה "זמן הוא שריר", שכוונתה להקדים ככל האפשר את הצנתור, והנחיה זו מעוגנת כיום בהנחיות של איגודי הקרדיולוגים בארצות הברית, באירופה וגם בישראל.
אלא שמחקר שפורסם לאחרונה בכתב העת הרפואי היוקרתי New England Journal of Medicine מאתגר את ההסכמה הזו. במחקר, שבדק כמעט 100 אלף חולים שטופלו ב-515 בתי חולים בארצות הברית, נמצא שהזמן הממוצע החולף מרגע הגעת המטופל לבית החולים לביצוע הצנתור ירד ל-67 דקות מאז שנת 1983 - אך למרות זאת שיעורי התמותה לטווח קצר לא השתנו.
לתוצאה הזו, אומרים קרדיולוגים מומחים, יש כמה הסברים אפשריים. אחד מהם הוא שלמרות שהתומכן המושתל בצנתור פותח את החסימה בכלי הדם הגדול שנפגע, ייתכן שבחלק מהחולים כלי דם קטנים יותר שמספקים את הדם לשריר הלב עדיין נותרים פגועים.
"נכון להיום אמצעי ההדמיה שבהם אנו משתמשים בצנתור לא מאפשרים לראות מה קורה בכלי דם קטנים אלה בתוך השריר עצמו, וייתכן בהחלט ששם טמון הסוד, שיאפשר לנו להשיג שיפור נוסף בתוצאות", אומר פרופ' גדי קרן, מנהל המערך הקרדיולוגי במרכז הרפואי תל אביב.
קראו עוד
התקף לב: איך לזהות שזה קורה - ומה הטיפול
פיתוח ישראלי: המכשיר שינבא אם תקבלו התקף לב
התקף לב: האם הוא קטלני יותר עבור נשים?
הסבר אפשרי אחר מגיע בכלל מתחום הכלכלה, והוא שהטיפול בחסימות בעורקים הפך למיטבי עד כדי כך שהוא הגיע כבר לשיא שממנו ואילך חל מה שמכנים כלכלנים "חוק התפוקה השולית הפוחתת". על פי חוק זה, שהוא אחד מעקרונות הכלכלה הבסיסיים, כשעסק הוא קטן, תפוקתו השולית עולה. אבל בנקודה מסוימת, כשהוא צומח וגדל, מתחילה התפוקה השולית להצטמצם.
תחום הקרדיולוגיה, שממוקם ב-50 השנים האחרונות בחוד החנית של החדשנות הטכנולוגית ברפואה ושיפור באיכות הטיפול, בהחלט נמצא בתור הזהב שלו. תומכנים ממגוון סוגים, קוצבי לב, ניתוחי מעקפים והשתלות לב הובילו לירידה משמעותית בתמותה ממחלות לב וכלי דם.
במצב כזה אולי אין זה מפתיע שחלה האטה בקצב הירידה הזו. ואולם נראה שברד הפיתוחים החדשים בתחום אינו פוסק, והמפתחים אינם שוקטים על שמריהם. הכתבה שלפניכם סוקרת כמה מהפיתוחים החדשים בתחום רפואת הלב, וגם פיתוחים מבטיחים שנמצאים עדיין בדרך.
מסתמים
החלפת מסתם באמצעות צנתור במקום ניתוח לב פתוח
עד לא מכבר חולים שסבלו ממחלה כלשהי באחד ממסתמי הלב ונזקקו לתיקון שלו או להחלפתו נאלצו לעבור ניתוח לב פתוח. אלא שחולים רבים לא יכלו לעמוד בניתוח הגדול הזה, הכרוך בפתיחת בית החזה ובעצירת פעולת הלב, וכתוצאה מכך חלק גדול מהם נדונו למעשה למוות בתוך שנים ספורות.
לנוכח זאת, אין זה מפתיע שהטכנולוגיה החדשה שפותחה בשנים האחרונות ומאפשרת לבצע החלפת המסתם או תיקונו ללא צורך בניתוח לב פתוח, הוכתרה על ידי הקרדיולוגים כאחת החשובות בתחום.
הטכנולוגיה פותחה בתחילה כדי לטפל במסתם האורטאלי – אחד מארבעת מסתמי הלב, שתפקידו לווסת את כמות הדם היוצאת מהלב אל אבי העורקים וממנו לשאר איברי הגוף. היצרות במסתם האורטאלי כרוכה בשיעורי תמותה גבוהים, של כ-40% בשנה הראשונה לאחר הופעת התסמינים ולמעלה מ-60% במהלך חמש שנים. מאחר שטיפול תרופתי אינו מעכב את ההיצרות, הטיפול המקובל בבעיה, ולמעשה הטיפול היעיל היחיד, הוא החלפת המסתם החולה במסתם תותב.
ואולם חלק גדול מהחולים הסובלים מהיצרות קשה של המסתם האורטאלי הם מבוגרים הסובלים ממגוון מחלות רקע משמעותיות נוספות, כך שהניתוח עצמו עלול לסכנם ולכן לא ניתן היה לטפל בהם. "האפשרות לבצע את החלפת המסתם בחולים אלה באמצעות צנתור במקום בניתוח לב פתוח היא התפתחות חשובה ביותר בתחום", קובע פרופ' רפאל ביאר, מנהל המרכז הרפואי רמב"ם וקרדיולוג מצנתר בהכשרתו.
"את מה שעשינו קודם לכן בניתוח גדול במשך שש שעות, אנחנו עושים עכשיו בחצי שעה בחדר הצנתורים. במהלך הטיפול מוחדר המסתם התותב אל תוך הצנתר ובאמצעותו מועבר אל מקומו הטבעי בלב. את הצנתר מחדירים דרך הרגל, או לחלופין: ישירות דרך חוד הלב. בקצה הצנתר מותקן גם בלון, ולאחר שממקמים את המסתם תוך שימוש בהדמיה, מנפחים אותו והוא מתחיל לתפקד מיד ומאפשר את זרימת הדם מהלב לאבי העורקים".
המסתם הראשון מסוג זה היה פרי פיתוחה של חברת סטארט-אפ ישראלית בשם PVT, שנרכשה מאוחר יותר על ידי החברה האמריקאית Edwards LifeSciences. בהמשך פותח מסתם נוסף, בעל יכולת להתרחב באופן עצמאי, ללא צורך בבלון, על ידי החברה הצרפתית-האמריקאית CoreValve. כיום הטכנולוגיה כלולה בסל הבריאות.
"ההצלחה המרשימה בטיפול במסתם האורטאלי הובילה לפיתוח טכנולוגיות חדשות שנועדו לטפל גם בבעיות של המסתם המיטראלי – המצוי בין החדר השמאלי והעלייה השמאלית", מסביר פרופ' ביאר. "זאת הן כדי להשתיל במקומו מסתם חדש, המותאם למקומו, או כדי לתקן דליפה שלו".
המסתם המיטראלי מורכב משני עלים שתפקידם למנוע חזרת דם מהחדר השמאלי של הלב לעלייה השמאלית; ממיתרים ומשתי קבוצות שרירים. מחלה בכל אחד מהמרכיבים האלה עלולה לגרום לתפקוד לקוי של המסתם.
אחת השכיחות שבהן היא דליפה, שבמצב חמור עלולה להוביל לאי ספיקת לב ואף למוות. גם במקרה זה תיקון הדליפה התאפשר בעבר רק באמצעות ניתוח לב פתוח, ואולם טכנולוגיה חדשה שפותחה בשנים האחרונות מאפשרת לבצע גם אותה באמצעות צנתור. הטכנולוגיה, שנקראת "מיטרה קליפ", מבוססת על קליפס מיוחד שבאמצעותו מצמידים את עלי המסתם - דבר הגורם לאיחוים ומאפשר ללב לשאוב דם ביתר יעילות. גם טכנולוגיה זו כלולה כבר כיום בסל.
היצרויות וחסימות
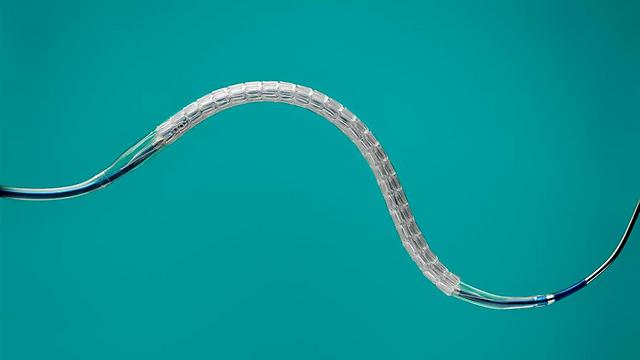
תומכנים מתוחכמיםהסטנטים הקיימים כיום בשוק מבוססים על סוג כלשהו של מתכת. הם מסייעים להשיג הטבה משמעותית לשנים ארוכות בקרב 70%-80% מהמטופלים, ואולם עדיין כ20%-30% מהמטופלים נזקקים להשתלה חוזרת באותו אתר שבו הושתל הסטנט כבר כעבור כחצי שנה בגלל היצרות חוזרת שהתפתחה בתוך הסטנט.
"כדי לפתור את הבעיה פותחו לפני למעלה מעשור סטנטים משחררי תרופה, שתפקידה למנוע את שגשוג התאים ולדכא את תהליך ההיצרות הנשנית", מסביר פרופ' ביאר.
"הם מבוססים על טכנולוגיות שונות שבאמצעותן התרופה מתחברת לתותב ומשתחררת ממנו. חלקם עשויים ממתכת בשילוב עם פולימר - חומר פלסטי המקשר בין הגוף המתכתי של התומכן לתרופה, שמטרתו לגרום לשחרור איטי ומבוקר של התרופה תוך חודש. תותב אחר מצופה בפולימר שהוא כשלעצמו נספג במשך חודש, ויחד עם ספיגתו משתחררת גם התרופה".
שני חידושים טכנולוגיים בתחום הם סטנט בעל מבנה מיוחד המאפשר לחבר את התרופה למתכת ללא צורך בפולימר מתווך, וסטנט מתכלה, העשוי כולו מפולימר הנספג בגוף ונעלם כולו ממנו עם הזמן. הטכנולוגיה הראשונה מתאימה בעיקר לחולים סוכרתיים, שכן הפולימר כשלעצמו עלול לעורר תגובה דלקתית מקומית אצלם ולעורר תהליך שבסופו תתפתח היצרות מחודשת בתוך הסטנט. דוגמה לסטנט כזה הוא Cre8, מתוצרת חברת CID, המשווק בארץ על ידי חברת גאמידה (נמצא בסל התרופות). בדפנות הסטנט מצויות שקערוריות שבתוכן מוטבעת התרופה המשתחררת לדופן העורק.
דוגמה לתומכן המתכלה הוא Absorb של חברת אבוט – שהוא גם הסטנט המתכלה משחרר התרופה הראשון שפותח. הסטנט הזה, שהושק לא מזמן בארץ, עשוי מפולימר המתמוסס באופן טבעי, שהשימוש בו נפוץ בשתלים רפואיים כמו תפרים מסיסים.
"בדומה לסטנט המתכתי, הסטנט המתכלה משמש כמעין "פיגום" השומר על כלי הדם פתוח", מסביר פרופ' ביאר. "ואולם, בתוך שישה חודשים עד שנה, הוא מתמוסס. הרעיון מאחורי הפיתוח הוא שלמעשה הסטנט צריך להחזיק את העורק פתוח למשך תקופה קריטית של כמה חודשים בלבד שבה העורק נוטה להיסגר. תקופה זו היא פרק הזמן הדרוש לעורק כדי להחלים באופן טבעי, ולאחר מכן הוא יישאר פתוח גם ללא התומכן.
זה בהחלט חידוש מעניין, ויש לו יתרונות. לדוגמה, אם יש צורך בניתוח מעקפים בהמשך קל יותר לטפל בעורק ללא ההפרעה של שתל קבוע. עם זאת, צריך יהיה לבחון בשנים הקרובות מהן התוצאות ארוכות הטווח שלו". לדברי היצרנית, הטיפול בתומכן המתכלה יהיה זמין בקרוב בבתי החולים לכלל המטופלים ללא עלות.
אי ספיקת לב
לב מלאכותי משודרג
עבור החולים שמצבם מתדרדר במהירות בעודם ממתינים להשתלת לב, פתרון זמני, המשמש כגשר עד שיימצא להם לב אנושי, הוא השתלת לב מלאכותי. זהו למעשה מעין מכשיר עזר המושתל בצמוד לחדר השמאלי הכושל (לא במקומו) ומחליף אותו בפעולתו.
ההשתלה הראשונה בארץ בוצעה כבר ב-1994, אך במשך למעלה מעשור הניתוחים האלה הוצעו רק כמוצא אחרון לחולים על ערש דווי, שכן הסיכון לסיבוכים לאחר ההשתלה היה גבוה והלב המלאכותי עצמו היה גדול ומסורבל, המשאבה שלו הייתה מחוץ לגוף וספק הכוח היה עצום בגודלו.
בשנים האחרונות הולכת הטכנולוגיה בתחום זה ומשתכללת. לפני כתשע שנים הושק בארץ מכשיר קטן ומתקדם יותר, אך עדיין מספר הניתוחים שבוצעו באמצעותו היה קטן מאוד. ב-2010 הושק מכשיר קטן ומתקדם עוד יותר, HeartWare, ומאז הולך ועולה מספר המושתלים של לבבות מלאכותיים, כשהוא עומד על כמה עשרות בשנה שחייהם ניצלים בזכות ההשתלה.
מסתם המווסת את מעבר הדם בין העליות
עם זאת, עבור חלק ניכר מהחולים הלב המלאכותי הוא עדיין פתרון זמני. פתרון חדש שהושק בארץ בחודשים האחרונים על ידי חברת V-Wave הוא מסתם זעיר המווסת את מעבר הדם בין עליות הלב, ועל ידי כך מסייע להפחתת הלחץ העודף הקיים אצל חולי אי ספיקת לב בעלייה ובחדר השמאלי, שגורם להצפת הריאות במים ולקשיי נשימה.
"באנשים בריאים, מעבר הדם בין העליות לחדרי הלב – מהעלייה הימנית לחדר הימני, ומהעלייה השמאלית לחדר השמאלי – מווסת במשטר לחצים מסודר למדי", מסביר פרופ' קרן, מי שהגה את הטכנולוגיה של V-Wave ואחד ממקימי החברה. "הלחץ בעלייה השמאלית אצל אדם בריא נע בין 8 ל-12 מילימטר כספית, ובעלייה הימנית בין 2 ל-5 מילימטר כספית. ואולם במצב של אי ספיקת לב הלחץ בעלייה השמאלית גבוה יותר, כך שנוצר למעשה הפרש לחצים מוגבר בין העלייה השמאלית לעלייה הימנית".
הרעיון שהבשיל במוחו של פרופ' קרן היה שפתיחת פתח קטן בין העלייה השמאלית לימנית עשויה אולי לעזור להפחית את הלחץ. "מניסיוני במרפאה ראיתי שגם אצל אנשים בריאים שיש להם פתח קטן בין העליות, כתוצאה מהפרש הלחצים יש במקרים רבים זרימה מהצד השמאלי, שבו הלחץ גבוה יותר, לצד הימני", הוא מסביר.
"באנשים שאצלם יש ממש חור משמעותי בין העליות, הזרימה משמאל לימין מוגברת עוד יותר. התצפיות האלה הביאו אותי למחשבה שאולי אם לחולה יש נטייה להעלות לחצים בצד השמאלי בגלל אי ספיקת לב, פתיחת פתח קטן בין העליות תוכל לעזור להפחית את הלחץ, משום שכאשר הלחץ יעלה - הדם יזרום לצד הימני. כשבדקתי את הספרות, מצאתי תיאורי מקרה של רופאים שאכן ניסו לעשות חור בין העליות לחולים עם אי ספיקת לב וראו שזה שיפר את מצבם".
בשנת 2000 הוא כתב פטנט על השיטה שפיתח, המבוססת על מסתם ביולוגי המוחדר באמצעות צנתור ומושתל בין העליות. לאחר שנוסה בהצלחה בבעלי חיים בוצעו עד כה 12 השתלות בבני אדם, שאחרי חלקם כבר קיים מעקב של שנה. גם בארץ כבר בוצעו שתי השתלות על ידי פרופ' רן קורנובסקי, מנהל מחלקת לב בבילינסון. "כמו בכל פיתוח חדש, בתחילה הוא ישמש רק לטיפול במצבים של אי ספיקת לב קשה, אבל אני מאמין שבסופו של דבר, הוא יוכל לשמש כפתרון גם בחולים קלים יותר", אומר פרופ' קרן.
טלאי לבבי
בכתב העת היוקרתי Nano Letters התפרסם לאחרונה מחקר המציג חידוש נוסף שעשוי להחליף בעתיד את השתלות הלב – טלאי לבבי המשלב ננו-חלקיקי זהב עם חומרים ביולוגיים מהחולה עצמו.
במחקר, שנערך על ידי ד"ר טל דביר והסטודנטית מיכל שבח מהמחלקה לביוטכנולוגיה, המחלקה למדע והנדסה של חומרים והמרכז לננו-מדע וננוטכנולוגיה באוניברסיטת תל אביב, ניסו החוקרים להנדס "טלאי" מתוחכם שיושתל בתוך הלב ויהווה תחליף לרקמת הלב שנפגעה כתוצאה מהתקף לב. "תאי הלב אינם מסוגלים להתרבות, ומאחר ששריר הלב מכיל תאי גזע מעטים בלבד, כשהתקף לב גורם ללב נזק משמעותי רקמת הלב אינה יכולה לרפא את עצמה," מסביר ד"ר דביר.
האתגר הראשון שעמד בפני החוקרים היה לייצר רקמה להשתלה שלא תידחה על ידי מערכת החיסון. לשם כך הם התבססו על שיטת עבודה המקובלת כיום במעבדות ברחבי העולם: גידול תאים שנלקחו מהחולים עצמם או ממקורות אחרים על גבי "פיגומים" תלת ממדיים.
פיגומים אלה מהווים תחליף לרשת הקולגן החוץ-תאית, שתומכת בתאי הלב בסביבתם הטבעית, בתוך הגוף. החידוש של החוקרים מאוניברסיטת תל אביב היה בחומר שממנו עשויים הפיגומים - רקמת שומן מבטנו של החולה עצמו.
"מדענים בעולם מנסים כיום להשתמש ברשתות חוץ-תאיות העשויות מרקמות של לב חזיר", אומר ד"ר דביר. "הבעיה היא שעל הרשתות האלה נותר משקע, והחשש הוא שמערכת החיסון של החולה תתקוף את החומרים ביולוגיים שנלקחו מהחי. לכן הצענו גישה חדשה – לקצור רקמת שומן היישר מבטנו של החולה עצמו, בהליך קל ופשוט יחסית, ואחר כך להרחיק ממנה את התאים ולהותיר רק את הרשת החוץ-תאית. פיגום כזה, העשוי מרקמות גופו של החולה עצמו, לא יעורר את מערכת חיסון שלו ולא יידחה על ידה".
המשימה הבאה הייתה לוודא שהרקמות המהונדסות מייצרות ומעבירות את אותם אותות חשמליים חיוניים הגורמים לשריר לב להתרחב ולהתכווץ. "החומרים הביולוגיים שלקחנו מהחולה כדי לבנות את הפיגומים הם בדרך כלל חומרים מבודדים, ולכן מפריעים להעברת אותות חשמליים ברשת הלבבית", מסביר ד"ר דביר. "כדי לפתור את הבעיה בחרנו להשתמש בזהב, חומר שמוליך חשמל מצד אחד, ומצד שני אינו יוצר אינטראקציה מזיקה עם רקמות הגוף".
כדי להשיג את האפקט הרצוי "עיטרו" החוקרים את הפיגומים הביולוגיים במשקע של ננו-חלקיקים של זהב, והגיעו לתוצאה מבטיחה - טלאים היברידיים המתכווצים ומתרחבים ומעבירים אותות חשמליים ביעילות ובמהירות. ניסויים ראשונים בחיות מעבדה הניבו ממצאים מעודדים, וכעת על החוקרים להוכיח שהטלאים הלבביים אכן משפרים את תפקוד הלב אחרי התקף לב ואינם נדחים על ידי מערכת החיסון. "בהמשך, נעבור לניסויים בחיות גדולות, ולאחר מכן אנו מקווים לעבור לשלב הניסויים הקליניים בבני אדם".
השתלת תאי גזע
במירוץ למציאת פתרון לבעיה של היעדר תחליף הולם לתאי שריר הלב הנמקים לאחר התקף לב, וגם לטיפול בהפרעות קצב או באי ספיקת לב – פתרון מרכזי נוסף שנמצא במרכז המחקר בשנים האחרונות הוא השתלת תאי גזע. בדרך זו מנסים חוקרים במעבדות רבות ברחבי העולם לשמר ואף להגדיל את מספר תאי שריר הלב הבריאים, לשפר את אספקת הדם ולהגביר את יכולת ההתכווצות של שריר הלב.
אחת המעבדות המובילות בתחום היא זו של פרופ' ליאור גבשטיין בטכניון, שהצליחו ב-2004 לייצר לראשונה מתאי גזע עובריים אנושיים קוצב לב ביולוגי. לאחר שהשתילו את תאי הגזע בליבו של חזיר שסבל מקצב לב איטי, מצאו החוקרים שהתאים האלה החלו לפעול כקוצב ביולוגי.
לצד מחקר זה פותחה במעבדה של פרופ' גפשטיין שיטה לייצור תאי גזע אנושיים מתאי גזע עובריים. "מדובר בטכולוגיה ייחודית מאוד, שבה נוטלים תאי גזע מעורו של החולה, הופכים אותם לתאי גזע עובריים, ומהם לתאי לב, ולאחר מכן ניתן להשתילם באותו חולה", מסביר פרופ' ביאר. המשמעות היא שניתן לגדל תאי לב עבור החולה מתאים שנלקחים ממנו עצמו, כך שהם ישמשו להחלפת תאי לב שעברו נמק לאחר התקף לב".
על אף ההצלחות המבטיחות, תחום השתלת תאי הגזע עדיין נמצא כיום בשלב של ניסויים במעבדה ובחיות, בעיקר חולדות. "מחקרים אלה מראים שהזרקה של תאים אלה לשריר הלב משפרת את תפקוד הלב, כאשר התאים מתחברים לתאי הלב האחרים והופכים למעשה לחלק מה'מנוע'", מסביר פרופ' ביאר. "ישנם כיום כבר כיוונים של חיות גדולות יותר, ואנו מקווים שבקרוב נגיע לשלב של מחקרים בבני אדם".
מחוברים מרחוק
מערכות ואפליקציות לניטור מצב חולי לב מרחוק
מלבד טכנולוגיות חדשניות אחד הנושאים החמים בתחום הקרדיולוגיה כיום הוא מערכות לניטור מרחוק של החולים. "דוגמה לכך היא שבבים שניתן להשתיל מתחת לעור, המודדים באופן רצוף את פעילות הלב ומשדרים אוטומטית למעבד שנמצא בכיסו של המטופל", אומר פרופ' ביאר. "במקרה של הפרעת קצב קשה הנתונים ישודרו אוטומטית דרך הסלולרי למוקד, כך שניתן יהיה להגיע לחולה במהירות ולטפל בו".
דוגמה נוספת היא מערכת home monitoring של חברת ביוטרוניק – מערכת מבוססת אינטרנט לניטור חולים שעברו השתלת קוצבי לב ודפיברילטורים. המכשיר המושתל בחולה מבצע מדידות אוטומטיות של אותם פרמטרים קליניים וטכניים הנבדקים במרפאה ומשדר אותם למשדר חיצוני. אם מתקבל ממצא חריג או שינוי קליני בעל פוטנציאל לסיכון חיי החולה, המערכת יוצרת התראה מיידית באתר הנגיש לצוות המרפאה, תוך דירוג אוטומטי של ההתראות על פי מידת דחיפות הטיפול בהן.
חידושים נוספים הם אפליקציות המתחברות לסלולר, ה"סופרות" את הנשימות של החולה ואף את כמות המים שהצטברו בריאות, ויכולות להתריע מבעוד מועד על הצטברות עודף מים בריאות ועל כשל של הלב, כך שהחולה יגיע במהירות לחדר המיון.
הכותבת היא בעלת דוקטורט (Phd.) בתקשורת בריאות ופוסט-דוקטורנטית בתחום תקשורת סיכונים בביה"ס לבריאות הציבור באוניברסיטת חיפה