מירוץ לחיים: מי יפתח ראשון תרופה לאבולה?
התפרצות האבולה באפריקה חשפה את המירוץ המטורף שמנהלות חברות שונות ברחבי העולם, וגם בישראל, לפיתוח תרופה וחיסון נגד הנגיף הקטלני. בשל חומרת המצב, מאשר ה-FDA שימוש בתרופות שטרם נוסו בבני אדם, ובעוד שאלפים מתים - חלק מהתוצאות מעודדות. מה הסיכוי שהמגיפה תסתיים?
בבוקר ה-22 ביולי האחרון התעורר ד"ר קנת ברנטלי, רופא אמריקאי שעובד במרכז לניהול מקרי אבולה בליבריה, כשהוא קודח מחום. ניסיונו המקצועי, כמו גם מקרי המוות שכבר דווחו בקהילה הרפואי, ביניהם זה של ד"ר סמואל בריסבן, אחד הרופאים הבכירים שהובילו את הטיפול באבולה בליבריה, הדליקו אצלו נורה אדומה.
חושש מפני הגרוע מכל, ברנטלי בודד את עצמו מיד. למרבה הזוועה, חששו התאמת. בדיקת דם שנערכה לו אישרה שהוא נדבק בנגיף האבולה הקטלני.
![]() עוד סיפורים חמים - בפייסבוק שלנו
עוד סיפורים חמים - בפייסבוק שלנו
עוד על מגפת האבולה:
![]() גיבורי האבולה: 120 רופאים ואחיות מתו מהנגיף
גיבורי האבולה: 120 רופאים ואחיות מתו מהנגיף
![]() מש' הבריאות נערך להתפרצות אבולה בישראל
מש' הבריאות נערך להתפרצות אבולה בישראל
![]() תקדים: FDA אישר תרופה לאבולה - שטרם נוסתה
תקדים: FDA אישר תרופה לאבולה - שטרם נוסתה
שלושה ימים מאוחר יותר אובחנה גם ננסי רייטבול, אחות אמריקאית שהייתה אחראית על תחנת השטיפה של יחידת הבידוד בבית החולים אלווה בליבריה, שבה אושפזו חולי האבולה. במסגרת תפקידה הייתה רייטבול אחראית לדאוג לכך שעובדי היחידה עוברים שטיפה וחיטוי בתמיסת כלור בהגיעם למחלקה המבודדת ובצאתם ממנה.
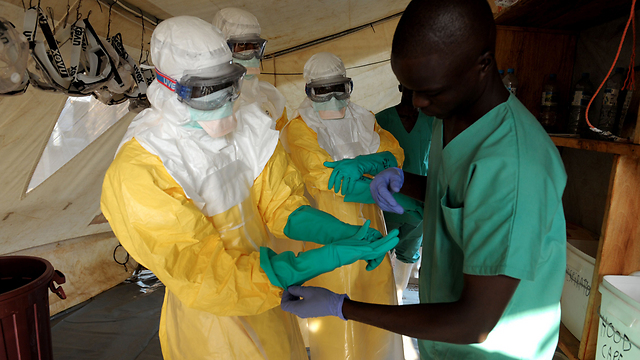
הן ברנטלי והן רייטבול לא הבינו כיצד נדבקו. שניהם הקפידו לעבוד בהתאם להנחיות הקפדניות שאושרו על ידי ה-CDC (המרכז לבקרת מחלות בארצות הברית). ברנטלי טיפל בחוליו כשהוא נראה כמעט כמו חוצן - לבוש בבגדים מיוחדים וכבדים, עוטה שלושה זוגות של כפפות, שערו מכוסה בברדס ועיניו עטויות מגיני עיניים מפלסטיק אטום. לרייטבול לא היה קשר ישיר עם מטופלים. כל זה, כאמור, לא עזר לשמור על בטיחותם.
עד מהרה החלו התסמינים המוקדמים האופייניים לאבולה להופיע אצל שניהם: חולשה, כאבי שרירים, כאבי ראש וגרון, הקאות ושלשולים. ההמשך המר נראה כמעט כבלתי נמנע. נגיף האבולה, אחד הקטלניים ביותר הידועים לעולם הרפואה, שההתפרצות האחרונה והקטלנית מכל עד היום שלו החלה בדצמבר האחרון, משתייך לקבוצת נגיפי הקדחת הדימומית. קבוצת נגיפים זו מכונה כך מאחר שהיא גורמת לדימומים חיצוניים ופנימיים, שבחלק הארי של המקרים מובילים למוות.
על פי מחקר שהתפרסם בכתב העת NEJM והתבסס על בדיקת דגימות דם מהחולים, נגיף האבולה האחראי להתפרצות הנוכחית במערב אפריקה משתייך לזן חדש, השונה בכ-3% מהחומר הגנטי שלו מהזן המכונה "זאיר", שהוא הזן הקטלני ביותר של הנגיף, והתמותה ממנו מגיעה עד ל-90%, כשההתדרדרות והמוות מהירים ביותר, לרוב תוך שבועיים. התסמינים הראשונים מתפתחים בהמשך לפגיעה במערכות רבות בגוף, כולל פגיעה בתפקוד הכליות והכבד.
ואכן, מצבם של ברנטלי ורייטבול הורע במהירות. הארגון שבמסגרתו פועלים השניים החליט לפנותם לארצות הברית לקבלת טיפול רפואי.

רגולציה של חמלה
נכון להיום לא קיימים תרופות או חיסונים לאבולה המאושרים לשימוש בבני אדם. עם זאת, שתי תרופות ניסיוניות נמצאות בשלבי מחקר מוקדמים יחסית בחיות, ובדרך לא דרך כלשהי הצליחו עמיתיהם של השניים להשיג במהירות אישור מה-FDA לתת להם אחת מהן במסגרת מה שמוגדר כ"טיפול חמלה", המאפשר זמינות לתרופות שנמצאות בתהליכי מחקר קליני.
אלא שמצב שניהם לא היה יציב דיו כדי שניתן יהיה להטיסם, לכן הוחלט להטיס אליהם את התרופה הניסיונית, שנקראת ZMapp. לשניים הוסבר שהיא מעולם לא נוסתה קודם לכן על בני אדם, אך הראתה הצלחה מבטיחה במחקרים קטנים בקופים, והם חתמו על טופס הסכמה מדעת, המבהיר כי הם מודעים לסיכון שבדבר.
בקבוקוני ה-ZMapp הגיעו לבית החולים בליבריה בבוקרו של יום שלישי, ה-29 ביולי. בשלב זה כבר היה מצבם של השניים קשה למדי, אולם היה עליהם להמתין לפחות עוד שמונה-עשר שעות עד שניתן יהיה להזריק להם את התרופה, שכן היא אוחסנה בהקפאה וההנחיות היו לאפשר לה להפשיר באופן טבעי.
בתחילה ביקש ברנטלי שרייטפול תקבל את המנה הראשונה שתפשיר, שכן בשל גילו הצעיר יותר הוא חשב שיש לו סיכוי טוב יותר להילחם במחלה. ואולם בשלב כלשהו באותו יום חלה החמרה קשה במצבו, עד כדי כך שהוא התקשה לנשום ונראה היה כי הוא גוסס.
הרופאים החליטו לתת לברנטלי את המנה הראשונה, והם הזריקו לו אותה באמצעות עירוי. תוך שעה התחולל לנגד עיניהם מה שהם הגדירו כלא פחות מ"נס": ברנטלי החל לנשום בקלות רבה יותר והפריחה על גופו נעלמה. בבוקר הבא הוא כבר היה מסוגל אפילו להתקלח בעצמו, לפני שעלה על מטוס הפינוי המיוחד שהביא אותו לבית החולים האוניברסיטאי אמורי בארצות הברית. את הגעתו, כשהוא יורד מהאמבולנס בתלבושת הבידוד הלבנה המיוחדת, תיעדו ברוב התרגשות כל כלי התקשורת העולמיים.
תגובתה של רייטפול לתרופה, שאותה קיבלה זמן מה אחרי ברנטלי, לא הייתה כה מרשימה בתחילה. ואולם כמה ימים אחר כך, לאחר שקיבלה את המנה השנייה, חל שיפור משמעותי גם במצבה, וגם היא כבר הייתה יציבה דיה כדי להתפנות בחזרה לארצות הברית.
על פי הדיווחים בתקשורת מצב שניהם ממשיך להשתפר. למרבה הצער, את חולה השלישי שטופל ב-ZMapp, הכומר הספרדי מיגל פחארס, הטיפול הניסיוני לא הצליח להציל והוא נפטר מהנגיף.
למרות זאת, קרוב לאלפיים האנשים שנדבקו עד כה בליבריה, גינאה, סיירה ליאונה וניגריה, מבקשים לעצמם לפחות את הסיכוי שהיה לכומר פחארס. את האור בקצה המנהרה מספקים כמה תרופות וחיסונים שנמצאים כיום בתהליכי מחקר ופיתוח. אף על פי שאף אחד מהם לא הגיע עדיין לשלב של מחקרים בבני אדם, מה שאומר שבטיחותן ויעילותן טרם הוכחו, באוגוסט האחרון הודיע ארגון הבריאות העולמי כי לנוכח מספר החולים והמתים הגדל בהתמדה, אין בעיה מוסרית במתן תרופות ניסיוניות לחולי אבולה.
"מצאנו את עצמנו בדילמה", הסבירה מארי פול קיני, עוזרת מנכ"ל ארגון הבריאות העולמי. "ישנם כמה תרופות וחיסונים חדשים שפותחו אך טרם נוסו בבני אדם. במקביל, יותר מדי חיים אבדו בינתיים".
הסרום הסודי
התרופה ZMapp, שזכתה בתקשורת העולמית לכינוי "הסרום הסודי", פותחה על ידי חברת ביוטכנולוגיה קטנה מסן דייגו בשם Mapp Biopharmaceutical Inc, במסגרת שיתוף פעולה עם שתי חברות נוספות, LeafBio ו-Defyrus Inc, במימון ממשלת ארצות הברית והסוכנות לבריאות הציבור בקנדה.
בשלב זה רב עדיין הלא ידוע על הידוע בנוגע לתרופה. מה שכן ידוע הוא שאפילו המחקרים בחיות נמצאים עדיין בשלבים מוקדמים. על פי מסמכי החברה, ארבעה קופים שהודבקו באבולה שרדו לאחר שקיבלו את התרופה תוך 24 שעות לאחר ההדבקה, ושניים מתוך ארבעה קופים אחרים שלהם ניתנה התרופה תוך 48 שעות לאחר ההדבקה שרדו אף הם. לעומת זאת, כל הקופים בקבוצת הביקורת מתו.
הפיתוח של ZMapp מבוסס על גישה המכונה אימונותרפיה פסיבית. במקום לייצר תרופה שממריצה את מערכת החיסון של החולה לייצר נוגדנים שיתקפו את הנגיף, באימונותרפיה פסיבית פשוט מזריקים לחולה את הנוגדנים עצמם. מדובר בנוגדנים חד שבטיים - נוגדנים שמקורם בשבט אחד של תאי מערכת החיסון, שהם נוגדנים ספציפיים כנגד הגורם המזיק שאליו מכוון הטיפול.
"הזרקת חומר שמעודד את הגוף ליצור נוגדנים מתאימה לטיפול במצבים שבהם יש זמן להמתין עד ליצירת הנוגדנים על ידי הגוף", מסביר פרופ' אלי שוורץ, מנהל המרכז למחלות טרופיות במרכז הרפואי שיבא, המשמש גם כנשיא האגודה הישראלית לפרזיטולוגיה ומחלות טרופיות ומראשי הארגון העולמי לרפואת מטיילים.
"לעומת זאת, כשהאדם כבר חולה ובמצב קשה, במקרים רבים אין זמן ויש צורך לנטרל את הפתוגן (הגורם המזיק) מהר ככל האפשר. מתן נוגדנים חד שבטיים כנגד הגורם הפתוגני משמשת ברפואה לטיפול במחלות זיהומיות שונות, כמו כלבת וטטנוס, וגם בסרטן. המקור לנוגדנים יכול להיות מדמם של אנשים או בעלי חיים. לדוגמה, בכלבת ניתן להפיק את הנוגדנים מדמם של אנשים שקיבלו את החיסון, או לחלופין: מסרום של חזירים".
ZMapp מבוססת על "קוקטייל" של נוגדנים המיוצרים באמצעות שימוש בעכברים ובעלי טבק. הרעיון אמנם נשמע כמו מרקחת של מכשפות, אבל מדובר בתהליך מתוחכם ביותר. ראשיתו בחשיפת עכברים לחלבון מפתח של נגיף האבולה. לאחר החשיפה אוספים את הנוגדנים שפיתחו העכברים והם עוברים תהליך של התאמה גנטית, כדי להפוך אותם לדומים יותר לנוגדנים האנושיים, וכך להקטין את הסיכון שיעוררו תגובה חיסונית כשיוזרקו לבני אדם.
תאורטית ניתן היה להשתמש כבר בנוגדנים אלה כתרופה הסופית, אולם כדי שאפשר יהיה לייצר את הנוגדנים בהיקפים גדולים פנו המדענים לכיוון מעניין: צמחים. הגן של כל אחד מהנוגדנים שהופקו מהעכברים ועברו התאמה לנוגדנים האנושיים הוחדר לעלי טבק, באמצעות מערכת מיוחדת שפותחה על ידי חברת אייקון גנטיקה הגרמנית. בעקבות זאת מייצרים העלים את הנוגדן הצמחי בתהליך שנמשך כמה שבועות בלבד, אז ניתן לקטוף אותם ולמצות מהם את הנוגדן.
"הפקת הנוגדנים מחיות מפחיתה מצד אחד את הסיכון להדביק את החולה במחלות אנושיות אחרות כמו איידס או צהבת", מסביר פרופ' שוורץ. "מצד שני היא מגדילה את הסיכון לתגובות אלרגיות. לכן, אם אכן מצליחים לייצר את הנוגדנים בטכניקה גנטית דרך צמחים זהו יתרון חשוב. בתהליך הגנטי משתמשים בנוגדנים המופקים מהעכברים רק בשלב הראשון, כשבהמשך מַרְבִּים בהתמדה את אותה כמות קטנה מקורית באמצעות השימוש בצמחים".
מי שמגדלת את הנוגדנים כיום במשתלות הטבק שלה היא לא אחרת מחברת הטבק האמריקאית ריינולדס - כיוון ייצור מפתיע שבו צועדות גם ענקיות טבק אחרות, כמו פיליפ מוריס, המשקיעות אף הן בטכנולוגיות לייצור תרופות מבוססות טבק. אף שהשימוש בעלי טבק מאפשר לייצר בקלות יחסית קילוגרמים של הנוגדנים הנחוצים, דווח כי ריינולדס עשויה להזדקק לכמה חודשים כדי להרחיב את מתקניה.
משתיקים את הגן של הנגיף
כארבע שנים טרם ההתפרצות במערב אפריקה ביצעה חברת תרופות קטנה אחרת מקנדה בשם טקמירה מחקר על קופי מעבדה שהודבקו במנה קטלנית של נגיף האבולה. המחקר, שפורסם בכתב העת Lancet, הראה שמתן שבע מנות של התרופה הניסיונית של החברה, TKM-Ebola, החל מחצי שעה לאחר ההדבקה ובימים שלאחריה, הביא ל-100% הישרדות של הקופים.
מחקרים פרה קליניים נוספים הדגימו 83% הישרדות כשהטיפול בתרופה החל 24 או 48 שעות לאחר ההדבקה, ו-67% הישרדות כשהוא ניתן 72 שעות לאחר ההדבקה. זאת בהשוואה ל-0% בקבוצת הפלצבו שלא קיבלה את התרופה.
ממצאים אלה מרשימים במיוחד לאור העובדה שהקופים נחשפו לזן האבולה זאיר, הזן הקטלני ביותר של הנגיף. בעקבות ההצלחה המרשימה בניסויי החיות עברה החברה לשלב הראשוני של ניסויים בבני אדם. בשלב זה, שנועד לבחינת בטיחות התרופה, אמורים היו להשתתף במחקר 28 מתנדבים בריאים. אלא שבסוף יולי, לאחר שהתרופה ניתנה ל-14 מתנדבים, הורה ה-FDA לעצור את המחקר בשל תופעות לוואי שנצפו אצל אחד מהם, בהן בחילה, צמרמורות, לחץ דם נמוך וקוצר נשימה.
רשות המזון והתרופות האמריקאית טענה שהתגובה מחייבת בחינה מחודשת של נושא הבטיחות, וביקשה מהחברה להעביר אליה מידע בטיחותי נוסף. ואולם, בעקבות המשך התפרצות הנגיף באפריקה ובלחץ דעת הקהל, חזרה בה ושינתה את מעמד הניסויים הקליניים בתרופה מ"עצירה מלאה" ל"עצירה חלקית" - מעמד המאפשר להמשיך במחקר אך רק בחולים המאובחנים כנגועים בנגיף האבולה ולא במשתתפים בריאים.
התרופה פועלת על ידי השתקת הגנים של נגיף האבולה באמצעות מנגנון שנקרא RNAi. "מדובר בגישה חדשה לפיתוח תרופות שבה משתמשים במנגנון ה-RNAi כדי לשתק באופן ספציפי גנים מסוימים שמעורבים במחלות שונות", מסביר פרופ' נווה.
מנגנון ה"הפרעה לרנ"א" נועד להגן על התא מפני נגיפים, והוא גם אחד ממנגנוני הבקרה על המתרחש בתא. מנגנון זה קיים באופן טבעי במרבית היצורים בעלי הגרעין, החל מצמחים ותולעים, וכלה בבני אדם, והוא אופיין לראשונה על ידי שני מדענים, אנדרו פייר וקרייג מלו, ב-1998. ב-2006 זיכתה אותם התגלית בפרס נובל לפיזיולוגיה ולרפואה.
בשנים האחרונות מסתמן השימוש ב RNAi כהבטחה הבאה בפיתוח תרופות בעלות יכולת השתקת חלבונים המעורבים במחלות קשות שונות שכיום אין להן תרופה, בהן מחלות סרטן ומחלות זיהומיות שונות, וחברות רבות עוסקות בתחום זה. ואולם עד כה לא אושרו עדיין תרופות המבוססת על המנגנון, וה-TKM עשויה להיות אפוא הראשונה.
התרופה הישראלית
במירוץ אחר התרופה לאבולה יש גם משתתפים ישראלים. מדענים מאוניברסיטת בן גוריון חוקרים כבר למעלה מעשור את האבולה ומנסים לפתח טיפול למחלה. מחקרם מתבצע במסגרת קבוצת מחקר שבה נוטלים חלק גם חוקרים אמריקאים, צבא ארצות הברית וארגונים נוספים.
התרופה שעל פיתוחה הם עמלים מבוססת על אותו מנגנון שבאמצעותו פועלת ה-ZMapp – נוגדנים חד שבטיים, רק שבמקום להשתמש בנוגדנים מחיות הם בחרו להשתמש בנוגדנים אנושיים המופקים מדמם של אנשים ששרדו את האבולה.
ד"ר לסלי לובל, סגן ראש המחלקה למיקרוביולוגיה, אימונולוגיה וגנטיקה באוניברסיטת בן גוריון, וד"ר ויקטוריה יאוולסקי, נסעו לאפריקה ואיתרו אנשים ששרדו את האבולה. הם נטלו תאים מדמם ויצרו מהם נוגדנים שמהם הם מתכוונים ליצור תרופה שתנטרל את הנגיף, ולהתחיל בקרוב בניסויים בבעלי חיים.
מהנדסים את הנגיף
נוסף על הניסיונות לפתח תרופות לאבולה מדענים במרכזים בעולם עובדים בשנים האחרונות על פיתוח חיסונים שיאפשרו להגן על האוכלוסייה ועל אנשי הצוותים הרפואיים מפני הנגיף. אחת הבעיות המרכזיות העומדות בפני החוקרים בפיתוח חיסון כזה היא מגוון הזנים של נגיף האבולה - מה שאומר שהחיסון צריך להיות כזה שיגן מפני כל הזנים, או לחלופין: שיש צורך לפתח חיסון נפרד לכל אחד מהזנים.
לפני כשבועיים הציע משרד הבריאות הקנדי לתרום לארגון הבריאות העולמי 1,000 מנות של חיסון ניסיוני שפותח על ידי סוכנות הבריאות הקנדית. החיסון, VSV-EBOV, פותח כנגד הזן הקטלני זאיר, שכאמור, הזן האחראי להתפרצות הנוכחית הוא מוטציה השונה ממנו במעט. בדומה לתרופות, גם חיסון זה עדיין לא נבדק בבני אדם, אך לדברי שרת הבריאות הקנדית רונה אמברוז, הניסויים שנערכו עד כה בקופים נראים מבטיחים.
"באמת לא ניתן לדעת עד כמה זה בטוח ומה עומדות להיות תופעות הלוואי", היא אמרה בריאיון לתקשורת. "אבל בנסיבות יוצאות דופן אלה באפריקה כיום, אנחנו מנסים לעשות כל מה שניתן כדי לסייע".
מנגנון הפעילות של חיסון ה-VSV-EBOV עדיין אינו ברור כל צרכו. אחת ההשערות היא שהוא מתחרה עם הנגיף על אתרי מטרה, וכך מונע ממנו לפלוש לתאים, להתרבות ולהתפשט. השערה נוספת היא שהוא מגרה את מערכת החיסון להגיב בחיסול הנגיף עם פלישתו לגוף.
החיסון אמור להינתן לפני החשיפה לנגיף האבולה, אך נטען שהוא יכול להגן גם כשהוא ניתן דקות לאחר החשיפה. עם זאת לא ידוע עדיין מהו המינון שצריך לתת כדי לספק הגנה לבני אדם, והמדענים עובדים כעת על חישוב והערכה של המינון הנחוץ על סמך המחקרים שנערכו בקופים.
המנות הראשונות אמורות להינתן לאנשי הצוותים הרפואיים באזורים הנגועים, שכבר הביעו את הסכמתם לקבל את החיסון. בינתיים נשלחו עשר מנות של החיסון לבית חולים ז'נבה, בהתאם לבקשת ארגון הבריאות העולמי וארגון רופאים ללא גבולות.
מלבד ה-VSV-EBOV, ארבעה חיסונים נוספים המצויים בשלבי פיתוח ומחקר מועמדים לזכות בתמיכה מהמכון הלאומי לבריאות בארצות הברית. החיסון שנמצא בשלב המתקדם ביותר הוא של חברת GSK הבריטית, בשיתוף עם המוסד הלאומי לאלרגיה ומחלות זיהומיות (NIAD). גם חיסון זה הראה תוצאות מבטיחות בניסויים שנערכו בקופים, והוא אמור להיכנס בקרוב לשלב הראשון של מחקר בבני אדם.
חיסון זה מבוסס על טכניקה של ריפוי גנטי - החדרת שני גנים של האבולה אל תוך נגיפים מסוג אדנו וירוס, שפועל כמעין נשא המחדיר את הגנים אל תוך הכרומוזומים של התאים. נגיפי האדנו וירוס גורמים למחלות נשימה ולזיהומים בעיניים ובמערכת העיכול, אך לצורך השימוש בהם בריפוי גנטי מסולקים מהם הגנים העלולים לפגוע בתאים הבריאים. ברגע ששני הגנים שנושאים האדנו וירוסים חודרים לתוך התא, הם מייצרים חלבון היוצר תגובה חיסונית בגוף כנגד האבולה.
"חיסונים המבוססים על הנדסה גנטית נחשבים לבטוחים יחסית, בשונה מכאלו המבוססים על נגיף מוחלש", מסביר פרופ' נווה. "החדרת הנגיף המוחלש עלולה לגרום לפיתוח מחלה מוחלשת, ואצל אנשים פחות בריאים אפילו את המחלה עצמה. לעומת זאת, בהנדסה גנטית הסיכון הזה לא קיים. למעשה, בטכניקה זו אפילו לא מחדירים את החומר הגנטי המלא של הנגיף אלא רק את חלקו. בדרך זו מפעילים את מערכת החיסון של האדם ומעוררים יצירת נוגדנים בגופו".
הישורת האחרונה
המירוץ המטורף להשגת תרופה כיום מדגיש בעיה חמורה בדרך שבה פועלים כיום מחקר ופיתוח התרופות: למרות שיעור התמותה הגבוה בקרב החולים, שמגיע עד לכדי 90% בחלק מזני האבולה, ועל אף הפחד הקמאי כמעט שמעוררת התפשטות המגיפה, עדיין מדובר במחלה שמשפיעה על כמות קטנה יחסית של אנשים - מה שאומר שלחברות התרופות אין תמריץ כלכלי להשקיע בפיתוח תרופות עבורן.
האור הירוק שנתן ארגון הבריאות העולמי לשימוש בתרופות ובחיסונים הניסיוניים מספק אומנם תקווה מסוימת לחולים ולאנשי הצוותים הרפואיים באפריקה, אולם נראה שהכמויות הקיימות, הן של ה-ZMapp, הן של ה-TKM-Ebolaוהן של חיסון ה-VSV-EBOV- שתי התרופות והחיסון שכבר זמינים, לא יעזרו משמעותית לעצור את המגיפה.
נכון להיום יכולת האספקה של החברות מוגבלת ועדיין עומדים בפניהן אתגרים לא פשוטים המקשים על הגדלה מיידית של היקף הייצור.