סרטן השד הוא הסרטן השכיח ביותר בקרב נשים. בכל שנה מאובחנות בו כ-2.3 מיליון נשים ברחבי העולם, וכ-5,000 מהן בישראל. אחת ההחלטות הקשות ביותר בטיפול בשלב מוקדם של המחלה היא האם להוסיף כימותרפיה אחרי הניתוח. מצד אחד, טיפול כזה יכול להשמיד תאי סרטן שנותרו ולהפחית את הסיכון לחזרת המחלה. מצד שני, לא בכל המקרים הוא באמת מועיל, ולעיתים הוא כרוך בתופעות לוואי קשות, פגיעה באיכות החיים ואף סיבוכים שעלולים להימשך זמן רב.
לכן, אחד האתגרים המרכזיים הוא לזהות כבר בשלב האבחון מי מהמטופלות באמת צפויה להרוויח מכימותרפיה. בהיעדר חיזוי מדויק, ההחלטות מתקבלות לא פעם תחת אי ודאות. התוצאה היא שחלק מהנשים מקבלות טיפול מיותר, בעוד אחרות עלולות לפספס טיפול שדווקא היה יכול לעזור להן.
2 צפייה בגלריה


מודל AI חדש מנתח דגימות מסרטן השד ומסייע לקבוע בתוך דקות אם כימותרפיה אכן תועיל למטופלת
(צילום: Shutterstock)
כיום קיימות בדיקות גנומיות, ובראשן בדיקת "אונקוטייפ שד", שמסייעות להעריך את הסיכון לחזרת המחלה ואת התועלת האפשרית מכימותרפיה. אך לבדיקות האלה יש חסרונות: הן יקרות, עשויות להימשך שבועות ואינן נגישות לנשים רבות ברחבי העולם. בנוסף, הן אינן מדויקות לחלוטין, ולכן לעיתים מובילות גם להחלטות טיפול לא מיטביות. כל אלה עומדים מאחורי המאמץ העולמי לפתח פתרונות מדויקים יותר, מהירים יותר ונגישים יותר.
הדילמה שמטרידה כל מטופלת
על רקע הצורך הזה פיתחנו בטכניון, יחד עם פרופ' דביר ארן מהפקולטה לביולוגיה, מודל חדשני. המודל מוצג במאמר שפורסם השבוע בכתב העת המדעי היוקרתי The Lancet Oncology והוצג גם בכנס החברה האירופית לאונקולוגיה רפואית ESMO. המודל פותח במעבדה לעיבוד גיאומטרי של תמונות, בשיתוף פעולה בין-פקולטי, בין-תחומי ובין-לאומי עם רופאים, ביולוגים ופתולוגים מהטכניון וממוסדות מובילים בישראל, בארצות הברית ובאירופה. הוא מתרגם צורך קליני אמיתי לפתרון חישובי שניתן ליישם בפועל.
 ד"ר גיל שמאי צילום: באדיבות דוברות הטכניון
ד"ר גיל שמאי צילום: באדיבות דוברות הטכניוןבאמצעות שילוב של בינה מלאכותית מתקדמת עם מומחיות קלינית, המודל יודע להעריך את הסיכון להישנות סרטן השד ואת התועלת הצפויה מכימותרפיה. זאת על בסיס דגימת רקמה שנלקחת ממילא מהגידול במסגרת האבחון הראשוני. מדובר בכלי חדשני שעשוי לקרב את הרפואה המותאמת אישית לשטח, ולהציע למטופלות פתרון מדויק יותר, מהיר יותר וזמין יותר.
מה רואים שהעין האנושית מפספסת
המודל החדש יודע לנתח תמונות של דגימות רקמה ברזולוציה גבוהה, ולבחון אזורים שונים של הגידול וסביבתו. הוא מזהה דפוסים חזותיים שמעידים על ההתנהגות הביולוגית של הסרטן, כמו קצב חלוקת התאים, צורתם, מבנה הרקמה שמעיד על אגרסיביות, סימנים לפעילות של מערכת החיסון ומאפיינים נוספים שיכולים להעיד על רגישות או עמידות לטיפול. בפועל, המערכת סורקת כמות עצומה של מידע ומזהה גם רמזים זעירים שרופא אנושי, מנוסה ככל שיהיה, לא יכול לקלוט ולנתח במלואם.
 פרופ' רון קימלצילום: באדיבות דוברות הטכניון
פרופ' רון קימלצילום: באדיבות דוברות הטכניוןהמחקר נשען על ההתקדמות המשמעותית ביכולת של בינה מלאכותית לנתח תמונות גדולות ומפורטות במיוחד. בעשור האחרון הצטבר ידע רב בפיתוח מודלים לניתוח דגימות פתולוגיות, ובמקביל נבנו מאגרי מידע גדולים של דגימות דיגיטליות, שהם הבסיס לאימון מערכות אמינות. המערכת שלנו אומנה על יותר מ-170 אלף דגימות, והגיעה למשימה עם "הבנה" רחבה של עולם הפתולוגיה. לאחר מכן היא נבדקה על אלפי מטופלות נוספות בבתי חולים בישראל, בהם כרמל, העמק ושיבא, וגם באוסטרליה ובארצות הברית, והראתה ביצועים עקביים גם בקרב אוכלוסיות שונות.
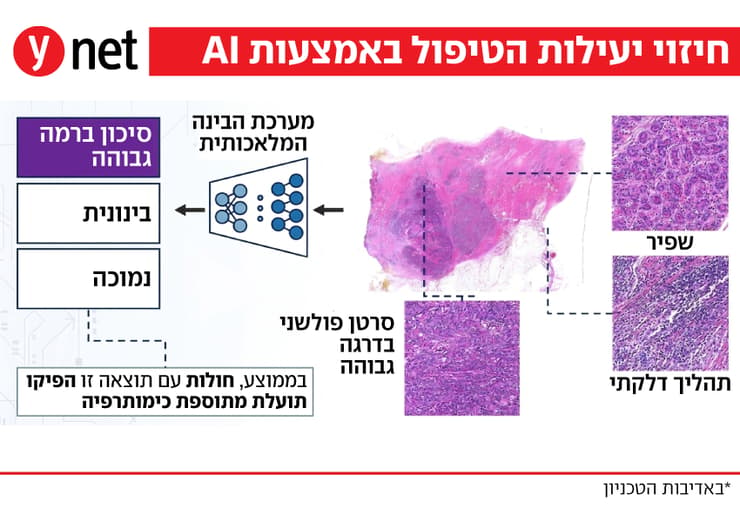
בניגוד לבדיקות גנומיות, המערכת מנתחת ישירות את תמונות צביעת הרקמה הסרטנית ומפיקה מהן "חתימה חזותית" שמסייעת לנבא מהו הטיפול המתאים ביותר. היא מצליחה לזהות גם מידע שרופאים ופתולוגים אינם יכולים להבחין בו. דגימת הרקמה, שנלקחת כבר בשלב האבחון, נסרקת דיגיטלית ומועברת באופן מאובטח לניתוח. בתוך דקות מתקבל ציון מספרי שמעריך את רמת הסיכון ואת הסיכוי להפיק תועלת מכימותרפיה. זהו כלי תומך החלטה, שמסייע לרופא ולמטופלת לקבל החלטה מדויקת יותר לגבי המשך הטיפול.
תוצאה תוך דקות, בלי בדיקה גנומית
השימוש במערכת הראה יכולת חיזוי מדויקת ועקבית באוכלוסיות שונות ובבתי חולים מגוונים. אחד הגורמים המרכזיים לכך הוא גישה ייחודית לנתונים ממחקר TAILORx, מהמחקרים הגדולים והמשמעותיים בעולם בתחום סרטן השד. מדובר בניסוי רחב היקף שכלל יותר מ-10 אלף מטופלות, ומאפשר לבדוק בצורה אמינה האם המודל אכן יודע לנבא תועלת מכימותרפיה, ולא רק להעריך את הסיכון הסטטיסטי לחזרת המחלה.
2 צפייה בגלריה


דגימת גידול בשד לאחר סריקה דיגיטלית, שממנה מופק ציון להערכת הצורך בכימותרפיה
(צילום: Shutterstock)
זהו מודל הבינה המלאכותית הראשון מסוגו שאומת ככזה שמסוגל לנבא תועלת מטיפול בסרטן השד על בסיס דגימות פתולוגיות. התהליך מהיר ואינו דורש בדיקה גנומית מורכבת או דגימה נוספת מעבר למה שנלקח ממילא. המשמעות היא בדיקה פשוטה יותר, מהירה וזולה, שניתן לבצע כמעט בכל מעבדה פתולוגית עם ציוד בסיסי וחיבור לאינטרנט.
במדינות מתפתחות, שבהן בדיקות גנומיות כמעט אינן זמינות, מדובר בפוטנציאל להרחיב משמעותית את הגישה לרפואה מותאמת אישית. גם במדינות מערביות הכלי עשוי לקצר תהליכים, להפחית עלויות ולשפר את הדיוק באבחון.
במקביל לקידום הטמעה בישראל ולניסויים קליניים במדינות נוספות, נעשים מאמצים לשפר עוד את דיוק המודל ולהרחיב אותו לסוגי סרטן וטיפולים נוספים. ההערכה היא שבעתיד הקרוב כלים מבוססי בינה מלאכותית יהפכו לחלק בלתי נפרד מתהליך קבלת ההחלטות באונקולוגיה וברפואה בכלל.
הכותבים הם ד"ר גיל שמאי, חוקר בכיר במעבדה לעיבוד גיאומטרי של תמונות רפואיות בפקולטה למדעי המחשב ע"ש הנרי ומרילין טאוב בטכניון, ופרופ' רון קימל, חבר סגל בכיר באותה הפקולטה






