במשך עשרות שנים נשען הטיפול בסרטן ערמונית מתקדם על עיקרון ביולוגי ברור: מאחר שרוב גידולי הערמונית זקוקים להורמוני מין זכריים, ובראשם טסטוסטרון, כדי לגדול ולשרוד, צריך לחסום מהם את מקור ההזנה הזה. הטיפול, המכונה דיכוי אנדרוגנים או לעיתים סירוס רפואי, מצליח במקרים רבים לכווץ את הגידול ולהאט את התקדמות המחלה.
אבל ההצלחה הזו לא תמיד מחזיקה לאורך זמן. אצל חולים רבים הסרטן לומד להסתגל, מפתח עמידות וממשיך להתקדם גם כאשר רמות הטסטוסטרון נמוכות מאוד. מחקר חדש בהובלת חתן פרס ישראל, פרופ' יוסף ירדן מהמחלקה לאימונולוגיה ורגנרציה ביולוגית במכון ויצמן למדע, שממצאיו מתפרסמים היום בכתב-העת המדעי EMBO Molecular Medicine, מציע כעת הסבר לאחד ממנגנוני הבריחה האלה: שינוי גנטי נפוץ, שמופיע בכמחצית ממקרי סרטן הערמונית, גורם לשני גנים שונים להתחבר זה לזה וליצור מעין גן חדש וחריג.
לפי המחקר, השינוי הזה מאפשר לתאי הגידול לעקוף את המסלול ההורמונלי שנחסם, ולהפעיל במקומו מסלול הישרדות חלופי הקשור לקורטיזול, הורמון הסטרס המרכזי של הגוף. ממצאים אלה מסמנים כיוון טיפולי חדש לחלק ניכר מהחולים בסרטן הערמונית, ומציבים גם תמרור אזהרה לגבי שימוש בסטרואידים במקרים מסוימים של המחלה.
סרטן הערמונית הוא אחד מסוגי הסרטן השכיחים ביותר בקרב גברים בעולם, וגם אחד הגורמים המרכזיים לתמותה מסרטן בגברים. המחלה מתפתחת בערמונית, בלוטה קטנה במערכת הרבייה הגברית שאחראית לייצור חלק מנוזל הזרע. ברוב המקרים מדובר בגידול שמתפתח באיטיות, אך ישנם גם סוגים אגרסיביים יותר, שעלולים להתפשט לאזורים אחרים בגוף, בעיקר לעצמות ולבלוטות הלימפה.
"הצמיחה וההישרדות של מרבית תאי סרטן הערמונית תלויות במידה רבה בהורמונים זכריים הנקראים אנדרוגנים, ובעיקר בטסטוסטרון ובנגזרתו הפעילה יותר, דיהידרוטסטוסטרון", מסביר פרופ' ירדן. לדבריו, הורמונים אלה מפעילים את הקולטן לאנדרוגנים, חלבון שמווסת גנים המעורבים בצמיחת תאים ובהישרדותם. "בשל תלות זו, הפחתת רמות האנדרוגנים או חסימת האיתות דרך הקולטן לאנדרוגנים מהוות את אבן היסוד בטיפול בסרטן הערמונית מזה עשרות שנים".

העיקרון הזה עומד בבסיס הטיפול המקובל במחלה מתקדמת: טיפול לדיכוי אנדרוגנים, או ADT, המכונה לעיתים "סירוס" רפואי או כירורגי. מטרתו היא להפחית באופן דרמטי את רמות הטסטוסטרון או לחסום את הקישור שלו לקולטן לאנדרוגנים, ובכך להאט את צמיחת הגידול. אלא שגם לטיפול הזה יש מגבלה משמעותית. "הטיפול הזה עשוי להיות יעיל מאוד בתחילה, לגרום להתכווצות הגידול ולהאט את התקדמות המחלה", אומר פרופ' ירדן. "עם זאת, אתגר קליני משמעותי הוא שרבים מהגידולים מסתגלים עם הזמן והופכים עמידים לטיפול".
"תאי הסרטן עשויים להגביר את ייצור הקולטן לאנדרוגנים או את רגישותו, לרכוש מוטציות שמאפשרות לקולטן להישאר פעיל גם בהיעדר הורמונים, לייצר אנדרוגנים בעצמם, או להפעיל מסלולי איתות חלופיים שעוקפים לחלוטין את התלות באנדרוגנים. המשמעות הקלינית של התהליך הזה דרמטית"
עמידות זו מתפתחת באמצעות מספר מנגנונים ביולוגיים. "תאי הסרטן עשויים להגביר את ייצור הקולטן לאנדרוגנים או את רגישותו, לרכוש מוטציות שמאפשרות לקולטן להישאר פעיל גם בהיעדר הורמונים, לייצר אנדרוגנים בעצמם, או להפעיל מסלולי איתות חלופיים שעוקפים לחלוטין את התלות באנדרוגנים", מסביר פרופ' ירדן. "המשמעות הקלינית של התהליך הזה דרמטית: הגידול, שבתחילה הגיב לדיכוי ההורמונלי, ממשיך להתקדם למרות הטיפול. שלב זה מכונה סרטן ערמונית עמיד לסירוס, או CRPC, והוא נחשב לרוב אגרסיבי יותר וקשה משמעותית לטיפול".
למעשה, התפתחות העמידות היא המגבלה המרכזית העומדת בפני הטיפולים ההורמונליים הקיימים כיום לסרטן הערמונית. "אף ש-ADT מסוגל לעכב את התקדמות המחלה, הוא לרוב אינו מרפא סרטן ערמונית מתקדם", מדגיש פרופ' ירדן. האתגר הזה עומד בלב המחקר בתחום: להבין כיצד נוצרת העמידות, לזהות את נקודות התורפה החדשות של הגידול, ולפתח אסטרטגיות טיפוליות שיוכלו למנוע אותה, לעכב אותה או להתגבר עליה לאחר שכבר הופיעה.
נתיב מילוט מסוכן
ואמנם, אחד הרמזים החשובים לפתרון חידת העמידות התגלה כבר לפני יותר משני עשורים. בשנת 2005 התברר כי אצל כמחצית מחולי סרטן הערמונית קיים שינוי גנטי המכונה tERG: גן מאוחה, שנוצר מחיבור לא תקין בין חלקים של שני גנים שונים. אף שמדובר באחד השינויים הגנטיים השכיחים ביותר בסרטן הערמונית, עד היום הוא לא שימש בפועל כמטרה לטיפולים אנטי-סרטניים מותאמים אישית, וגם לא נוצל כסמן ביולוגי שמכוון החלטות טיפוליות באונקולוגיה.
כאן נכנסה השאלה המרכזית של המחקר החדש. "השערתנו הייתה שנוכחות הגן המאוחה יכולה לקבוע את תגובת החולים לטיפולים אנטי-הורמונליים", מסביר פרופ' ירדן. "במילים אחרות, חסימת tERG או שותפיו עשויה למנוע את הופעת העמידות לטיפולים הורמונליים אצל חלק מחולי סרטן הערמונית".
על אפשרויות הטיפול בעתיד: "מבחינה מעשית, אנו מציעים אסטרטגיית טיפול תרופתית אפשרית לגידולי ערמונית חיוביים ל-tERG: טיפול משולב בו-זמני בתרופות החוסמות הן את AR - המסלול המרכזי לצמיחת הגידול, והן את GR - מסלול המילוט"
כדי לבדוק זאת, החוקרים פנו תחילה לנתונים שכבר נאספו בחולים. בשיתוף פעולה עם המכון הלאומי לסרטן בארצות הברית NCI, בבת'סדה, מרילנד, הפועל במסגרת המכונים הלאומיים לבריאות NIH. הם בחנו תוצאות שפורסמו מניסויים קליניים שבהם נעשה שימוש בתרופות החוסמות את הקולטן לאנדרוגנים המכונה AR. הניתוח העלה ממצא חשוב: תגובת המטופלים לתרופות האנטי-הורמונליות הייתה פחות טובה כאשר tERG היה נוכח בגידולים שלהם.
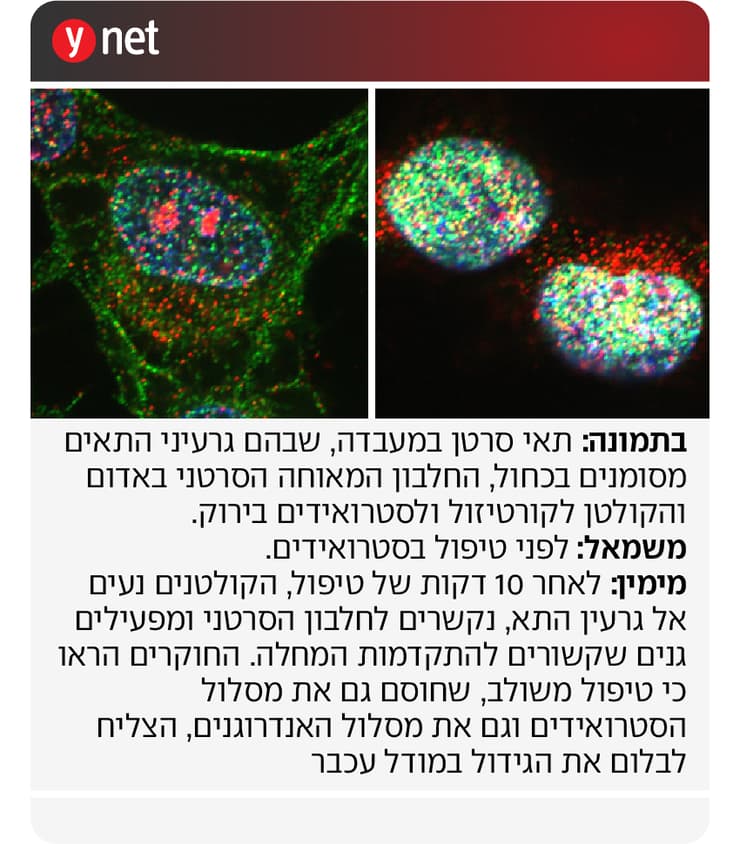
השלב הבא נועד להבין מה בדיוק עושה אותו גן מאוחה בתוך תא הסרטן. החוקרים ביצעו ניתוח ביוכימי של tERG ומצאו כי הוא מסוגל להיקשר לקולטן הורמונלי אחר, הקולטן לגלוקוקורטיקואידים המכונה GR. גלוקוקורטיקואידים הם משפחה של הורמונים סטרואידיים, שהמוכר שבהם הוא קורטיזול - הורמון הסטרס המרכזי של הגוף. במילים פשוטות, כאשר התרופות חוסמות את המסלול המרכזי של האנדרוגנים, אותו גן מאוחה מאפשר לתאי הסרטן להפעיל מסלול חלופי, מעין נתיב מילוט ביולוגי, שדרכו הם יכולים להמשיך לשרוד.
אלא שכאן מתגלה גם הפרדוקס המרכזי של המחקר. במצב רגיל, כאשר הורמוני המין הזכריים עדיין פעילים, הם מדכאים את פעולתם של קולטני הקורטיזול, ולכן המסלול הזה נותר מושתק. אבל כאשר הטיפול מדכא את הורמוני המין או חוסם את פעולתם, אותה בלימה מוסרת. במצב הזה, הגן המאוחה יכול להפעיל את מסלול הקורטיזול, ולאפשר לסרטן להמשיך להתקדם למרות הטיפול שנועד לעצור אותו.
כדי לבחון את המנגנון הזה במודל חי, השתמשו החוקרים, בהובלת ד"ר ארונצ'אלאם סקאר, בדגימות מגידולים אנושיים, חלקן חיוביות ל-tERG וחלקן שליליות, והשתילו אותן בעכברים. הניסויים אישרו את ההשערה: חוסמי הקולטן לאנדרוגנים היו יעילים רק כאשר tERG לא היה מבוטא בגידול. לעומת זאת, כאשר tERG היה מבוטא, החוקרים הצליחו לעכב את הגידול רק באמצעות שילוב של שתי תרופות - אחת שחוסמת את הקולטן לאנדרוגנים, ואחת שחוסמת את הקולטן לגלוקוקורטיקואידים. לפי החוקרים, במודל העכבר הטיפול המשולב דיכא את הגידול לאורך זמן והוביל להארכת חיים.
בדרך לטיפול מותאם אישית
הממצאים האלה מחדדים את משמעותו של אותו שינוי גנטי נפוץ. לדברי פרופ' ירדן, אף שכמחצית מהגברים המאובחנים עם סרטן הערמונית מקבלים בשלב כלשהו של מחלתם טיפול אנטי-אנדרוגני, התצפיות במחקר מצביעות על כך שחולים שהגידולים שלהם חיוביים ל-tERG עמידים מלכתחילה יותר לטיפול זה.
"על פי ממצאינו, המנגנון העומד בבסיס תופעה זו כולל קישור ישיר של החלבון המאוחה tERG לקולטן לגלוקוקורטיקואידים, GR אשר מספק לתאי הסרטן מסלול חלופי להישרדות כאשר AR נחסם", מסביר פרופ' ירדן. כלומר, כאשר התרופה חוסמת את המסלול המרכזי שעליו נשען הגידול, תאי הסרטן החיוביים ל־tERG מצליחים להפעיל מסלול אחר, שמאפשר להם להמשיך לשרוד.

מכאן נובעת גם המשמעות המעשית של המחקר. "מבחינה מעשית, אנו מציעים אסטרטגיית טיפול תרופתית אפשרית לגידולי ערמונית חיוביים ל-tERG: טיפול משולב בו-זמני בתרופות החוסמות הן את AR - המסלול המרכזי לצמיחת הגידול, והן את GR - מסלול המילוט", אומר פרופ' ירדן. עם זאת, הוא מדגיש כי לא מדובר בגישה שמתאימה בהכרח לכל חולה. "חשוב לציין שחולים שאינם מבטאים tERG עשויים שלא להפיק תועלת משילוב תרופתי זה, שכן מסלול המילוט אינו קיים בגידוליהם".
מעבר לפוטנציאל הטיפולי, למחקר יש גם משמעות קלינית נוספת: הוא מעלה צורך בזהירות במתן סטרואידים לחלק מחולי סרטן הערמונית. כיום סטרואידים משולבים במקרים רבים בטיפול בסרטן ערמונית מתקדם, בין היתר כחלק מפרוטוקולים טיפוליים קיימים. ואולם, מאחר שסטרואידים מפעילים את הקולטן לגלוקוקורטיקואידים, המחקר מצביע על אפשרות שבגידולים חיוביים ל-tERG הם עלולים דווקא לסייע להפעלת מסלול המילוט של הסרטן.
"חשוב גם להיזהר במתן סטרואידים לחולים אלה, שכן הם מפעילים את הקולטן לקורטיזול ועלולים לסייע לסרטן", אומר פרופ' ירדן. לדבריו, תרופה שחוסמת את הקולטן לקורטיזול, והראתה במחקר תוצאות מבטיחות בעכברים, כבר אושרה באחרונה על ידי ה-FDA לטיפול בחולות עם סרטן השחלה. "כולי תקווה שההצלחה תשוחזר גם בסרטן הערמונית".
המשמעות היא שבעתיד ייתכן שהטיפול בסרטן הערמונית ייקבע לא רק לפי שלב המחלה או מידת התפשטותה, אלא גם לפי הפרופיל הגנטי של הגידול. חולים שליליים ל-tERG צפויים להמשיך לקבל את הטיפול הסטנדרטי המקובל כיום, בעוד שחולים חיוביים ל-tERG עשויים להיות מועמדים לשילוב של טיפול המכוון לקולטן לאנדרוגנים עם מעכבי הקולטן לגלוקוקורטיקואידים.
"כעת ניתן יהיה לנסות את הטיפול המשולב בחולים אנושיים עם הגן המאוחה", אומר פרופ' ירדן. במובן הזה, המחקר אינו רק מסביר מדוע טיפול ותיק ומרכזי בסרטן הערמונית מפסיק לעבוד אצל חלק מהחולים, אלא גם מציע דרך אפשרית להתגבר על אותה עמידות. אם הממצאים יאושרו בהמשך במחקרים קליניים בבני אדם, בדיקת tERG עשויה להפוך מכלי מחקרי לסמן שיסייע לקבוע מי יוכל להסתפק בטיפול ההורמונלי המקובל, ומי יזדקק כבר מההתחלה לחסימה כפולה של שני מסלולי ההישרדות של הגידול.