אילו מדענים היו יכולים להשתחל לצוללת מיקרוסקופית ולשייט בין תאי הגוף, כמו בסרט "המסע הפנטסטי" מ-1966, אחת התחנות הראשונות שלהם ודאי הייתה הכבד. מבנהו הייחודי של האיבר הפנימי הגדול בגופנו כולל יחידות פעולה קטנות דמויות משושה הנקראות "אוּניות" (lobules), המבצעות כל אחת יותר מ-500 פעולות שונות במקביל, מה שהופך את הכבד לא רק לאיבר חיוני, אלא לאחת ממערכות העבודה המרשימות והמורכבות ביותר שהטבע בנה.
כעת, זה אפשרי. באופן וירטואלי, לפחות. במחקר חדש שהתפרסם לאחרונה בכתב-העת המדעי Nature, מציגים לראשונה מדעני מכון ויצמן למדע ועמיתיהם במרכז הרפואי שיבא ובמאיו קליניק בארה"ב אטלס גנטי של הכבד האנושי הבריא ברזולוציה של 2 מיקרון. הממצאים חושפים כי חלוקת התפקידים בכבד האנושי שונה מביונקים אחרים וענפה יותר ממה שהיה ידוע עד כה, ומראים כיצד היא הופכת אזורים מסוימים בכבד שלנו לפגיעים במיוחד לכבד שומני.
"הכבד הוא האיבר הפנימי הגדול ביותר בגוף האדם, והוא אחראי על תפקידים רבים", מסביר ד"ר אורן יעקובובסקי, מתמחה בכירורגיה כללית במרכז הרפואי שיבא ודוקטורנט במכון ויצמן, מצוות החוקרים. "הכבד אחראי על הפעילות המטבולית בגוף, על ייצור חום, על ייצור חלבונים, על מערכת הקרישה ועל סינון של רעלים - הוא יודע לקחת תרופות ורעלים מהדם, לשנות את התצורה שלהם ולהפריש אותם מהגוף. הוא אחראי גם על משק הסוכר בגוף יחד עם הלבלב".
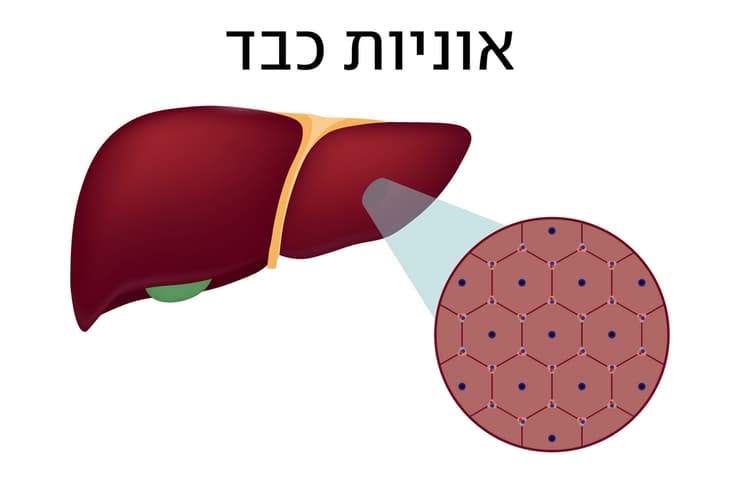
אותה מורכבות לא מתרחשת בקנה מידה גדול, אלא דווקא ברזולוציה זעירה במיוחד. "הכבד בנוי מיחידות תפקודיות מאוד קטנות שנקראות אוניות", הוא מוסיף. "הדם זורם ממערכת העיכול אל הכבד ונכנס לאונית, שנראית כמו משושה, דרך כלי דם קטנים שנמצאים בהיקף שלה. משם הוא זורם פנימה אל המרכז, ומשם הוא זורם לכל הגוף. בתוך האונית הזאת למעשה מתבצעות כל הפעולות של תאי הכבד על הדם".
כבר מאז שנות ה-70 וה-80 ידוע כי תאי כבד מחלקים ביניהם את התפקידים הרבים בהתאם למיקומם בתוך כל תת-יחידה, אך הטכנולוגיה דאז אפשרה לקבל תמונה מעורפלת בלבד של חלוקה זו. "פשוט היו לוקחים דגימת כבד, חותכים אותה ובוחנים אותה תחת מיקרוסקופ", אומר ד"ר יעקובובסקי. באותה תקופה אף נמצא כי לאונית כמה אזורים שונים. "בחלק החיצוני הדם מאוד עשיר בנוטריינטים וחמצן וככל שמתקדמים יותר פנימה, נעשה שימוש בנוטריינטים האלה על ידי תאי הכבד כך שהדם שמגיע למרכז האונית הוא דם משומש, דם עני יותר", הוא ממשיך. "כתוצאה מכך ניתן להבחין בשינוי בין החלק החיצוני לפנימי. זה משהו שהיה ידוע. בשל כך, עד אז היה נהוג לחלק את זה האונית לשלושה אזורים שונים – מהחיצוני לפנימי".

"אטלס" חדשני
בשנים האחרונות הלכה והתפתחה טכנולוגיה שמאפשרת לזהות אילו גנים פעילים בכל תא ותא תוך מיקומם המרחבי המדויק של התאים על מפת הרקמה. עם זאת, למרות היכולות החדשות, מיפוי מדויק של חלוקת התפקידים בכבד האנושי התעכב, לא מעט בשל הקושי להשיג דגימות כבד מאנשים בריאים. בקבוצתו של פרופ' שלו איצקוביץ' במכון הבינו שהמפתח לפתרון הוא תרומות כבד אלטרואיסטיות; לכבד יכולת התחדשות מופלאה המאפשרת לאנשים לתרום חלק גדול ממנו לאדם הסובל ממחלה. כך בעזרת פרופ' עדו נחמני ופרופ' ניב פנקוביץ' מהמערך לכירורגיה כללית במרכז הרפואי שיבא וד"ר טימוצ'ין טאנר ממרכז ההשתלות של מאיו קליניק במינסוטה, ארה"ב, השיגו המדענים שמונה דגימות מתורמים בריאים והרכיבו "אטלס" של ביטוי גנטי בכבד האנושי.
6 צפייה בגלריה


מימין: פרופ' שלו איצקוביץ', פרופ' עדו נחמני, ד"ר אורן יעקובובסקי, פרופ' ניב פנקוביץ וד"ר טימוצ'ין טאנר
"ממש עד לפני כמה שנים, כדי לאפיין מה תא עושה, היית צריך להסתכל עליו במיקרוסקופ,לצבוע אותו, לראות למה הוא מגיב ואיך הוא מתנהג, אך מאז פרויקט ריצוף הגנום האנושי ישנן שיטות מתקדמות שמאפשרות לנו לקרוא חומר גנטי שיש בתא הנקרא RNA", ממשיך ד"ר יעקובובסקי. "כך אנחנו יכולים לאפיין אותו ברמה עמוקה יותר – אילו חלבונים יש שם, מה הוא יודע לעשות. אותו ריצוף הביא ממש למהפכה. אם פעם חשבנו שכל תא כבד עושה את אותן פעולות, היום אנחנו יודעים להגיד שיש הרבה סוגים של תאים שעושים עבודות שונות כתלות במיקום שלהם בתוך אותה אונית".
למעשה, אותו גילוי אפשר לחוקרים לראשונה לראות את הכבד ברזולוציה שלא הייתה זמינה עד היום - לא רק כאיבר אחד, אלא כמערכת מורכבת של אזורים שונים, שכל אחד מהם מתפקד באופן ייחודי. "אלפי גנים התגלו כפעילים ברמות שונות בתאי כבד במקומות שונים, מה שמעיד על ארגון פנימי מדויק ומורכב בהרבה משחשבנו", אומר פרופ' איצקוביץ'.
פרופ' איצקוביץ':"במקום החלוקה לשלושה אזורי פעילות, שמקובלת כבר עשרות שנים, האטלס חשף שמונה אזורים בעלי תפקידים מובחנים. המיפוי מאפשר לכל מעבדה בעולם לצלול לעומק הכבד ולחקור מדוע אזורים שונים פגיעים למחלות שונות. מחלות מטבוליות, למשל, נוטות להתחיל במרכז האונית, בעוד שדלקות נגיפיות ואוטואימוניות מופיעות בעיקר בשוליה"
"במקום החלוקה הגסה לשלושה אזורי פעילות, שמקובלת כבר עשרות שנים, האטלס חשף שמונה אזורים בעלי תפקידים מובחנים. המיפוי המדויק של הכבד מאפשר כעת לכל מעבדה בעולם לצלול לעומק הכבד ולחקור מדוע אזורים שונים פגיעים למחלות שונות. מחלות מטבוליות, למשל, נוטות להתחיל במרכז האונית, בעוד שדלקות נגיפיות ואוטואימוניות מופיעות בעיקר בשוליה. כמו כן, לסרטן כבד ולגרורות מסרטנים אחרים יש את המקומות המועדפים עליהן. המפתח להבין מדוע זה כך מצוי במידע הגנטי המדויק שאספנו".
הפריצה הזו לא נולדה רק מטכנולוגיה מתקדמת, אלא גם מנקודת תורפה עמוקה במחקר: עד היום, למדענים פשוט לא הייתה מפה אמינה של כבד אנושי בריא להשוות אליה. "עד עכשיו לא היה לנו 'אטלס' של כבד אנושי בריא שיהווה רפרנס בריא שאפשר לעבוד עליו, ממש כמו ספר מפות ממוחשב", מאשר ד"ר יעקובובסקי. "חשוב שיהיה לך רפרנס של כבד בריא שממנו תוכל לצאת ולחקור את כל המחלות".
פריצת דרך זו הינה ייחודית משום שעד כה כל הכבדים המתוארים בספרות המחקרית לא הגיעו מתורמים בריאים. "כל הכבדים בספרות הם כבדים מתורמים של אנשים שעברו מוות מוחי ותורמים את איבריהם, אך מוות מוחי יכול להשפיע גם על הכבד. כבדים נוספים שהשתמשו בהם היו מאנשים שעברו ניתוח לכריתת גידול כבדי, ובאותם ניתוחים דגמו דגימה מאזור בריא ליד הגידול. אנחנו ערערנו את התפיסה הקיימת וטענו ששתי השיטות האלה הן לא מספיק מדויקות. אנחנו הראשונים שאפיינו את הכבד האנושי מדגימות בריאות, והדרך היחידה להשיג את זה היא מאותם תורמי כבד. עכשיו, למשל, מי שחוקר וירוסים בכל מקום בעולם יכול להיכנס לאטלס שלנו ולנסות לחפש היכן הווירוס שלו ישפיע הכי הרבה".
הכבד האנושי פועל אחרת
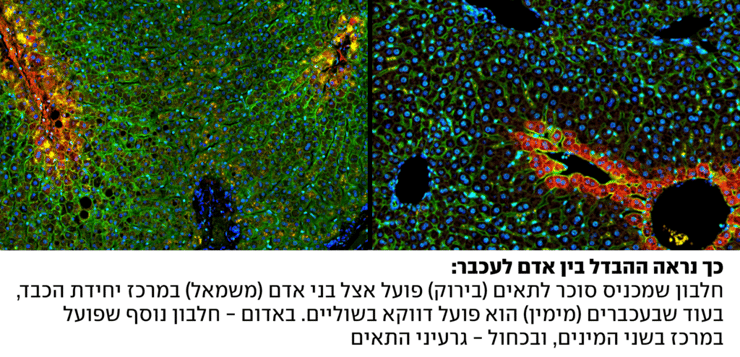
כדי להשוותם לבני-אדם, מיפו במעבדתו של פרופ' איצקוביץ' גם את הכבד הבריא בעכבר וכן ביונקים גדולים יותר, חזיר ופר, שלהם קצב חילוף חומרים וגודל אוניות כבד הדומים לאדם. כאמור, בכל היונקים דם זורם באונית מהשוליים למרכז ומספק בדרך חמצן ומזון לתאים. כתוצאה ממסלול זה, בשוליים שוררים תנאי שפע ובמרכז מחסור. בכל היונקים שנבדקו, למעט האדם, תנאי המחסור במרכז האונית גרמו לכך שהתאים שם יהיו יחסית פעילים פחות, בעוד באדם התגלה כי מתבצעות בליבת האונית פעולות רבות, ובהן ייצור שומנים מעודפי אנרגיה, הרכבת סוכר מחומרים שאינם פחמימות בזמני רעב, סינון רעלים וייצור נוזל המרה שמסייע בעיכול.
הבדל בולט נוסף שהתגלה במחקר בין הכבד האנושי לזה של יונקים אחרים נוגע לאגירת סוכר. הכבד מתפקד כ"מכל הדלק" של גופנו באמצעות ספיגה יעילה של הסוכרים שאנו מעכלים בארוחות ושחרורם באופן מבוקר בין הארוחות. במחקר התגלה שבאדם ספיגת הגלוקוז ייחודית למרכזי האוניות ולא לשוליהן, כמו בעכבר.
"חלוקת התפקידים הזו היא ברכה וגם קללה", מסביר פרופ' איצקוביץ'. "היא מאפשרת לכבד שלנו לאגור פחמימות ביעילות: תאים במרכז האונית קולטים ואוגרים סוכר (גלוקוז) ישירות מהדם, בעוד שתאים בשוליים ממירים לקטט לגלוקוז וכך תורמים גם הם למאגרי האנרגיה שמשמשים אותנו בצום. ואולם, חלוקת העבודה היעילה לא תוכננה לתזונה המודרנית ששופעת שומנים ופחמימות, ועשויה להסביר מדוע אנו נוטים לצבור שומן עודף במרכז אונית הכבד ולסבול מהצטלקות שלו".
ד"ר יעקובובסקי: "זה חשוב כי בכל העולם לא עובדים על רקמות אדם, שמאוד קשה להשיג, עובדים בעיקר על עכברים, חזירים או יונקים אחרים. אם לדוגמה חברת תרופות עובדת על פיתוח תרופה ובודקת אותה על מודל עכבר, היא כעת יכולה לבדוק באטלס שלנו ולראות היכן מתבטאים הגנים עליהם הם עובדים, בעכבר וגם בבן אדם"
כדי להתמודד עם השחיקה ולמנוע מחלה, התפתח במרכזה של אונית הכבד האנושי מנגנון תחלופה ייחודי. "גילינו שבבני-אדם, בשונה מיונקים אחרים, סוג אחד של תאי חיסון מעדיף את ליבת האונית במקום לעמוד על המשמר בשוליה – שער כניסת הדם לרקמה", אומר ד"ר יעקובובסקי. "תאי 'קופפר' הם תאים בולעניים שמסוגלים להגן מזיהומים אך גם לבלוע, לפרק ולמחזר שאריות תאים שהתבלו. אנו משערים שהם 'עברו למרכז' באדם כדי להתמודד עם השחיקה המוגברת".
להשוואה הזו יש חשיבות מרכזית, שכן מחקר רפואי רב מתבסס על מודלים של בעלי חיים, והבדלים בינם לבין האדם עשויים להשפיע על פרשנות הממצאים. "זה חשוב כי בכל העולם לא עובדים על רקמות אדם, שמאוד קשה להשיג, עובדים בעיקר על עכברים, חזירים או יונקים אחרים", מוסיף ד"ר יעקובובסקי. ״אם לדוגמה חברת תרופות עובדת על פיתוח תרופה ובודקת אותה על מודל עכבר, היא כעת יכולה לבדוק באטלס שלנו ולראות היכן מתבטאים הגנים עליהם הם עובדים, בעכבר וגם בבן אדם".
איך מתפתח כבד שומני מבפנים
בחלקו האחרון של המחקר הראו המדענים כיצד האטלס החדש מסייע להתחקות אחר התפתחות מחלות. הם התמקדו במחלת הכבד השומני המטבולי, מצב נפוץ המקושר לעודף משקל וסוכרת אך מופיע בדרגות שונות בכ-25% מהאוכולוסייה העולמית, שבו שומן מצטבר בכבד ועלול להוביל לדלקת ולהצטלקות. כל זאת התאפשר בזכות שיתוף הפעולה המיוחד עם מרכז ההשתלות של מאיו קליניק במינסוטה, ארה"ב. "לקחנו דוגמיות כבד בריאות מתורמים אנושיים - אנשים שעברו בירור מאוד משמעותי והוכח שהם בריאים. אולם בגלל תפוצת מחלת הכבד השומנית חלק מהתורמים הציגו שלבים מוקדמים של כבד שומני".
במילים אחרות: הייחוד של הדגימות הללו אפשר לחוקרים להסתכל לא רק על מחלה מתקדמת, אלא גם על נקודת ההתחלה. "עד עכשיו הרבה מקומות שחקרו כבד שומני חקרו כבד שומני מתקדם", ממשיך ד"ר יעקובובסקי, "עבדנו עם דגימות של אנשים שהיה להם כבד שומני בשלב התחלתי שעדיין נחשב בריא. ככה הצלחנו לתפוס את השלבים הראשונים המוקדמים של המחלה ואפיינו את הגנים שבאים לידי ביטוי".
ד"ר יעקובובסקי: "אנחנו מקווים שהבסיס הזה יהיה הרפרנס לכל עבודות הכבד בהמשך, כלומר כל מעבדה או חוקר שירצו לפתח תרופות, או לבדוק מחלות מסוימות, ישתמשו באטלס שלנו כדי לבדוק את התוצאות שלהם: מפיתוח תרופות ועד אפיון של מחלות מסוימות בכבד, האטלס שלנו יהווה בסיס להתחיל ממנו את המחקר"
החוקרים השוו בין תאים בריאים בכבד לבין תאים שהחלו לצבור שומן וגילו מספר דברים מפתיעים. "גילינו מנגנון הגנה", אומר ד"ר יעקובובסקי. "תאים שהתחילו להשמין בעצם כיבו גנים שגורמים לקליטת שומן והפעילו גנים אחרים שגורמים לפירוק שלו. כלומר, הכבד ממש מנסה להגן על עצמו בשלבים הראשונים מאותה ספיגת שומן בתוך התאים הכבדיים". עם זאת, הם גם מצאו כי בכבד האנושי יש כשל שמגביל את יכולתו להתנגד להשמנה ביעילות: התברר שהצטברות שומן מובילה לירידה בייצור חלק מהרכיבים במיטוכונדריה - אברונים שמפרקים שומנים".
אחרי שנים שבהן הרפואה התבוננה בכבד כאיבר אחד, המפה החדשה חושפת מציאות מורכבת בהרבה, כזו שעשויה לשנות גם את הדרך שבה ננסה לתקן אותו. "על בסיס המיפוי המדויק של הכבד, ניתן יהיה בעתיד לפתח טיפולים שממוקדים בגנים שגורמים לאזור מסוים להיות פגיע במיוחד למחלה ספציפית", אומר פרופ’ איצקוביץ’. "יתרה מכך, המודל של בניית אטלס גנטי ברזולוציית תא בודד מדגימות של תורמים בריאים ניתן ליישום באיברים נוספים, שעד כה לא מופו במדויק באדם, וייתכן שהוא ישנה מהותית את האופן שבו אנו מבינים את מבנה ותפקוד הגוף האנושי".
אחרי כל שכבות המורכבות, ההשוואות בין מינים והניסיון להבין היכן בדיוק מתחילה המחלה, החוקרים מבקשים להשאיר אחריהם גם משהו בסיסי יותר: תשתית. כזו שתוכל לשמש מעתה חוקרים אחרים, בכל מקום בעולם, כנקודת ייחוס אמינה לחקר הכבד האנושי. "אנחנו מקווים שהבסיס הזה יהיה הרפרנס לכל עבודות הכבד בהמשך, כלומר כל מעבדה או חוקר שירצו לפתח תרופות, או לבדוק מחלות מסוימות, ישתמשו באטלס שלנו כדי לבדוק את התוצאות שלהם", מכריז ד"ר יעקובובסקי. "מפיתוח תרופות ועד אפיון של מחלות מסוימות בכבד, האטלס שלנו יהווה בסיס להתחיל ממנו את המחקר".
במחקר השתתפו גם ד"ר קרן בהר הלפרן, ספיר שיר, רוי נובוסלסקי, ד"ר עדי אגוזי, ד"ר טל ברקאי, ד"ר יותם הרניק, ד"ר עמיחי אפריאט וד״ר יעל כורם כהנים מהמחלקה לביולוגיה מולקולרית של התא במכון; ד"ר חן מאיר וד"ר רון פרי מהמרכז הרפואי שיבא תל השומר; ד"ר רובן הופלין מאוניברסיטת פרייבורג, גרמניה; עפרה גולני, ד"ר אינה גוליאנד, ד"ר יוסף אדדי, ד"ר מירב קדמי וד"ר הדס קרן שאול מהמחלקה לתשתיות מחקר מדעי החיים במכון; ד"ר ליאת פלוס-אליגור, ילנה פריצ'יסלוב ודאנה הירש מהמחלקה למשאבים וטרינריים במכון.