בשנים האחרונות הפך קטמין לאחד הטיפולים המסקרנים ביותר בתחום הפסיכיאטריה. התרופה, שפותחה במקור כחומר הרדמה, נמצאה יעילה בהפחתה מהירה של תסמיני דיכאון - במיוחד בקרב אנשים הסובלים מדיכאון עמיד לטיפול. למרות השימוש ההולך וגובר בה, המנגנון הביולוגי המדויק שבאמצעותו היא משפיעה על המוח עדיין אינו מובן לחלוטין. לפחות עד עתה.
מחקר חדש שנערך ביפן ופורסם בכתב העת המדעי Molecular psychiatry מקבוצת Nature מספק כעת הצצה מפורטת לתהליכים המולקולריים המתרחשים במוח בעקבות טיפול בקטמין. במסגרת המחקר הצליחו חוקרים לראשונה למדוד במוח האנושי החי את השינויים בקולטני AMPA - חלבונים חשובים המעורבים בתקשורת בין תאי עצב.
דיכאון עמיד לטיפול (Treatment-Resistant Depression) הוא מצב שבו מטופלים אינם מגיבים באופן מספק לטיפולים התרופתיים המקובלים. ההערכות הן כי כ-30% מהאנשים הסובלים מדיכאון משתייכים לקבוצה זו, מה שמדגיש את הצורך בפיתוח טיפולים חדשים ויעילים יותר.
במחקר השתתפו 34 מטופלים שאובחנו עם דיכאון עמיד לטיפול, לצד 49 נבדקים בריאים ששימשו כקבוצת ביקורת להשוואה. הנתונים נאספו במסגרת שלושה ניסויים קליניים נפרדים שנערכו ביפן. כדי לבחון את המנגנונים הביולוגיים המעורבים בטיפול, השתמשו החוקרים בטכנולוגיית הדמיה מתקדמת מסוג PET-CT - שיטה המאפשרת למדוד תהליכים ביוכימיים במוח החי.
ד"ר אהוד רוזיצקי: "החוקרים גילו שככל שכמות הרצפטורים של גלוטומט במוח היא נמוכה יותר, ככה יש יותר סיכון לדיכאון עמיד לתרופות. הם הראו שקטמין היא תרופה שעובדת על הרצפטורים לגלוטומט - בתוך המוח, וגם את דרך הפעולה של התרופה - דרך שיפור המוליכות של גלוטומט"
קולטני AMPA הם חלק ממערכת הגלוטמט - אחת ממערכות התקשורת המרכזיות במוח. הם ממלאים תפקיד חשוב בפלסטיות עצבית, כלומר, ביכולתם של קשרים בין תאי עצב להשתנות ולהסתגל. במהלך המחקר החוקרים ביצעו סריקות PET למטופלים לפני תחילת הטיפול ולאחר סיום סדרת עירויי הקטמין שניתנו במהלך תקופה של כשבועיים. באמצעות שימוש בסמן רדיואקטיבי ייעודי המאפשר למדוד באופן ישיר את צפיפותם של קולטני AMPA על פני תאי העצב הם השוו בין הסריקות ובחנו כיצד הטיפול משפיע על צפיפות הקולטנים במוח.
השלב הראשון במחקר כלל השוואה בין מטופלים עם דיכאון עמיד לבין אנשים בריאים, כדי לזהות הבדלים בסיסיים בצפיפות הקולטנים. לאחר מכן בדקו החוקרים כיצד משתנה צפיפות הקולטנים לאחר טיפול בקטמין, והאם השינויים הללו קשורים לשיפור בתסמיני הדיכאון. התוצאות הראו כי במוחם של המטופלים נמצאו הבדלים אזוריים בצפיפות קולטני AMPA בהשוואה לנבדקים הבריאים. בנוסף נמצא כי הטיפול בקטמין לווה בשינויים בצפיפות הקולטנים במספר אזורים במוח.
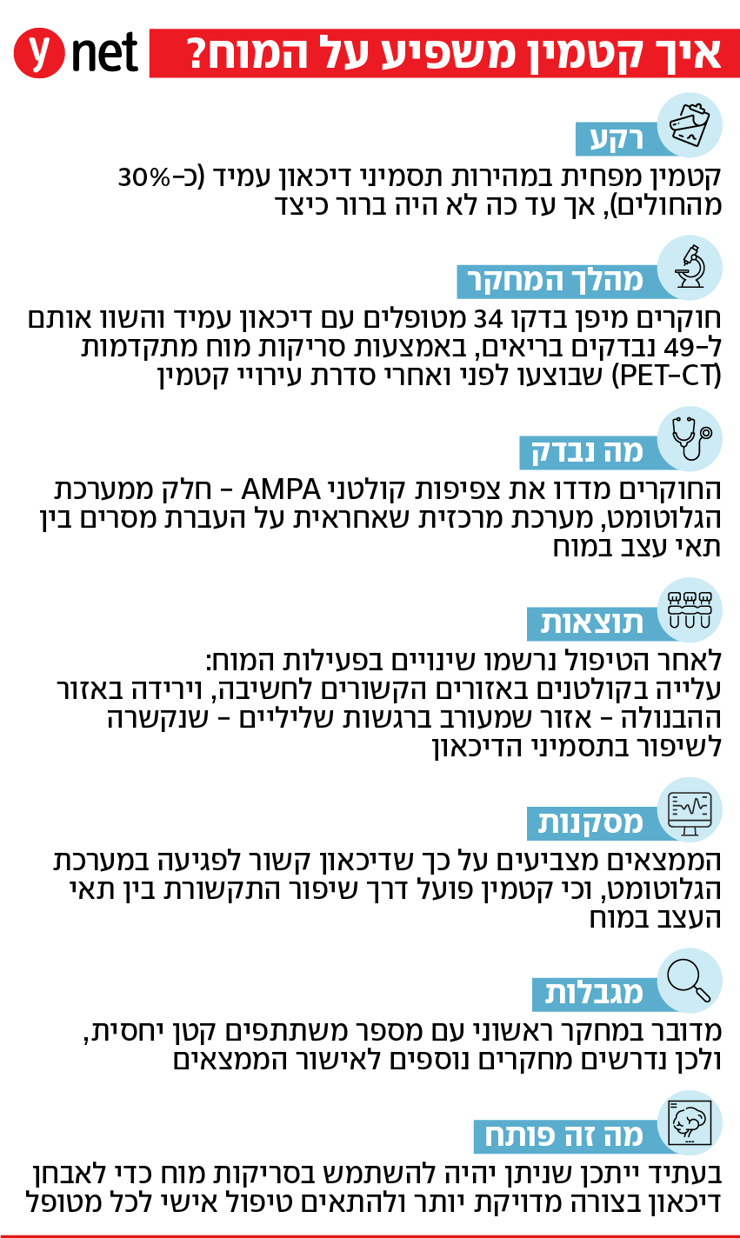
בחלק מאזורים שונים בקליפת המוח - השכבה החיצונית של המוח שאחראית בין היתר על חשיבה, קבלת החלטות ועיבוד מידע - נצפתה עלייה במספר הקולטנים לאחר הטיפול. לעומת זאת, באזורים אחרים במוח הקשורים לעיבוד רגשות ולתחושת תגמול, ובמיוחד באזור קטן בשם הבנולה (habenula) - אזור שמקושר לעיבוד רגשות שליליים ולתחושת אכזבה - נמצאה דווקא ירידה במספר הקולטנים. ירידה זו הייתה קשורה לשיפור בתסמיני הדיכאון אצל המטופלים. לדברי החוקרים, הממצאים מספקים עדות ישירה לכך ששינויים במערכת קולטני AMPA עשויים להיות אחד המנגנונים הביולוגיים שבאמצעותם פועל הקטמין. היכולת למדוד שינויים אלה במוח החי עשויה לסייע בעתיד בפיתוח טיפולים חדשים המכוונים לאותה מערכת עצבית.
הבנה גדולה יותר של מנגנון הדיכאון
המחקר מוסיף נדבך חשוב להבנת הפעולה של קטמין במוח, ומדגים כיצד טכנולוגיות הדמיה מתקדמות יכולות לחשוף מנגנונים ביולוגיים שהיו עד כה קשים למדידה בבני אדם. ד"ר אהוד רוזיצקי, פסיכיאטר ומנהל מערך בריאות הנפש בכללית מחוז ירושלים, אומר כי אחד הדברים שהופכים אותו לחריג הוא לא רק התוצאה - אלא גם הדרך שבה הוא בוצע. "המחקר השתמש בשיטות של הדמיה מוחית מאוד מתקדמת שנקראת PET-CT", הוא אומר ומסביר כי מדובר בכלים שמוכרים כיום בעיקר מתחום האונקולוגיה: "בתחום הפסיכיאטריה עדיין לא משתמשים בהם, בעיקר כי מדובר במכשירים מאוד יקרים וההפעלה מאוד יקרה - אבל זו טכנולוגיה שבאמת מסמלת את העתיד".
 ד"ר אהוד רוזיצקיצילום: כללית
ד"ר אהוד רוזיצקיצילום: כלליתבהמשך לכך, מתייחס רוזיצקי למערכת הגלוטומט - אחד הנוירו-טרנסמיטורים המרכזיים במוח, שעליו פועל הקטמין - ושנמצאה במחקר כגורם מרכזי הן בהתפתחות הדיכאון והן באופן שבו הטיפול משפיע עליו. "נוירו-טרנסמיטורים הם מוליכים עצביים האחראים על התקשורת בין מרכזי מוח שונים ובין תאי עצב", הוא אומר, "לכן ברור שמדובר בחומרים מאוד חשובים ובעלי השפעה גדולה על מחלות מוח ונפש. החוקרים גילו שני ממצאים מרתקים: הם גילו שככל שכמות הרצפטורים של הגלוטומט היא נמוכה יותר, ככה יש יותר סיכון לדיכאון קשה – דיכאון עמיד לתרופות. בנוסף הם הראו שקטמין היא תרופה שעובדת על הרצפטורים לגלוטומט - וגם את דרך הפעולה של התרופה, דרך שיפור המוליכות של גלוטומט".
כדי למקם את הממצאים בהקשר רחב יותר, רוזיצקי מצביע גם על השינוי בגישה המדעית להבנת דיכאון בעשורים האחרונים. "עד לשנים האחרונות התיאוריה המובילה בדיכאון הייתה התיאוריה הסרוטונרגית", הוא מסביר, "תיאוריה שאמרה שדיכאון קשור לירידה בפעילות של סרוטונין בתוך המוח, ועל בסיס התיאוריה הזו פותחו התרופות נוגדות הדיכאון, ה-SSRI, שמעלות את הסרוטונין".
לדבריו, למרות שהתרופות הללו אכן מסייעות לחלק מהמטופלים, הן אינן נותנות מענה לכולם. "אנחנו יודעים שיש דיכאון שהוא בדרך כלל קשה יותר - דיכאון עמיד לטיפול תרופתי. בערך 30%-40% מהמטופלים שסובלים מדיכאון מז'ורי לא יגיבו טוב לתרופות הקונבנציונליות של ה-SSRI. הגילוי שלגלוטומט יש השפעה גם על הפרעות דיכאון הביא גם להכנסת השימוש בקטמין", הוא אומר, "במקור זו בכלל תרופת הרדמה. כיום משתמשים בה להרדמה וטרינרית. יש לה המון תופעות לוואי בעייתיות, אבל ההכנסה שלה לטיפול בדיכאון הביאה לתוצאות יפות בכל הנושא של דיכאון עמיד לתרופות".
להבין דיכאון לעומק
אך בעוד שהמחקר וההסברים הביולוגיים מציעים הצצה מרתקת למה שמתרחש ברמת המולקולה והמעגלים העצביים, התמונה המלאה של דיכאון רחבה ומורכבת בהרבה. "דיכאון זו ההפרעה השכיחה ביותר בפסיכיאטריה והשכיחות שלה עולה", מסבירה ד"ר עידית גוטמן, פסיכולוגית קלינית מהחוג לפסיכולוגיה באוניברסיטת תל אביב. "היא מתרחבת גם כלפי מטה, גם לגילים צעירים יותר ויותר, וגובה מחיר מאוד כבד – לא רק בסבל האנושי: אפילו ברמה הכלכלית. זה עול רציני. אנשים שחולים בדיכאון לא מממשים את פוטנציאל ההשתכרות שלהם ופגיעים יותר לכל מיני מחלות, ולכן זו בעיה גדולה. איגוד הבריאות העולמי ממש מגדיר את זה כסוג של מגפה".
ד"ר עידית גוטמן: "משנת 2006 התרופה הזו אושרה לשימוש ציבורי. התחילו את הניסויים בצורה מאוד הדרגתית כשהשיח היה שהאפקט הוא מאוד דומה לנזעי חשמל במובן הזה שהוא אפקט מהיר לטווח קצר. גם נזעי החשמל וגם הקטמין ממש כמו עושים ריסט, כמו שעושים למחשב, למערכת העצבים המרכזית. זה נותן איזשהו פסק זמן מהכאב וסיכוי לטיפול פסיכותרפי"
בניגוד לתפיסה הרווחת, דיכאון אינו מצב שחולף מעצמו במהירות. "ללא טיפול, המשך של אפיזודה דיכאונית ממוצעת הוא כשנה, וגם לאחר מכן הוא עובר רק בכארבעים אחוז מהמקרים", ממשיכה ד"ר גוטמן, "זה אומר שברוב המקרים אנשים שסובלים מדיכאון עלולים לא להתאושש כמו שצריך. כלומר, יש בערך עשרים אחוז שמתאוששים רק חלקית".
 ד"ר עידית גוטמן פסיכולוגית קלינית, אוניברסיטת תל אביבצילום: שחר שחר, אוניברסיטת תל אביב
ד"ר עידית גוטמן פסיכולוגית קלינית, אוניברסיטת תל אביבצילום: שחר שחר, אוניברסיטת תל אביבבהמשך לכך היא מתייחסת גם לאופן שבו דיכאון עלול להפוך למצב כרוני ומתמשך. "אם דיכאון לא טופל, הוא עלול להתקבע ולהפוך למשהו מאוד עקשן. ההתוויה היא שאם אחרי פעמיים של אפיזודה דיכאונית יש פעם שלישית, יש להתייחס לדיכאון כאל מצב כרוני כמו סוכרת או לחץ דם ולקחת באופן קבוע את הטיפול התרופתי. בהקשר זה ניתן לציין תיאוריה הנקראת 'היפותזת הצלקת' שבעצם אומרת שדיכאון לאחר שני אפיזודות כנראה כבר פגע ברקמת המוח בצורה מספיק משמעותית כדי שהוא יהפוך את האדם לפגיע יותר להישנות".
על הרקע הזה, היא מציינת גם את המקרים שבהם דיכאון הופך לעמיד לטיפול - אותה תופעה שעמדה במוקד המחקר. "ההגדרה הרשמית לדיכאון עמיד היא דיכאון שבזמן שיא הגל הדיכאוני לא מגיב לטיפול התרופתי. רוב האנשים מגיבים לטיפול התרופתי, יש כאלה יותר ויש כאלה פחות. אנשים שסובלים מדיכאון חווים כאב נפשי בעוצמה מייסרת בצורה קיצונית. אם שני סוגי כדורים, כלומר שני טיפולים פרמקולוגיים שפונים למנגנונים קצת שונים במוח, לא מועילים להם בכלל – הדבר נחשב כבר כדיכאון עמיד. במקרה זה פונים לשיטות שהן קו שלישי. בדרך כלל טיפול בנזעי חשמל, שהיה נחשב לתקווה האחרונה לאנשים שלא מגיבים לתרופות בזמן שיא הכאב של הדיכאון".
עם זאת, לדבריה, כניסת הקטמין לשימוש שינתה במידה מסוימת את התמונה. "משנת 2006 התרופה הזו אושרה לשימוש ציבורי. התחילו את הניסויים בצורה מאוד הדרגתית כשהשיח היה שהאפקט הוא מאוד דומה לנזעי חשמל במובן הזה שהוא אפקט מהיר לטווח קצר. גם נזעי החשמל וגם הקטמין ממש כמו עושים ריסט, כמו שעושים למחשב, למערכת העצבים המרכזית. זה נותן איזשהו פסק זמן מהכאב וסיכוי לטיפול פסיכותרפי".
האפקט הזה, היא מסבירה, אינו עומד בפני עצמו, אלא יוצר חלון הזדמנויות שמאפשר למטופלים להתחיל תהליך טיפולי עמוק יותר. "אנחנו יודעים שטיפול בדיבור, של גלי קול דרך האוזניים, משנה את המסלולים המוחיים. יש צילומי סריקות מוח של אנשים לפני ואחרי טיפול בדיבור - וזה פועל. זה גם מחסן במידה מסוימת מפני הישנות - מנפילה מחדש לדיכאון. כדי להגיע לזה בן אדם צריך להיות מסוגל לפקוח את העיניים ולדבר, מה שקשה לעשות בדיכאון חמור. הפוטנציאל של קטמין נתן לנו עוד רמז למה קורה במוח ברמה הכימית-ביולוגית במצב של דיכאון. עד עכשיו הכרנו שני מסלולים עיקריים: השיטה של להעלות את רמת הדופמין והסרוטונין במוח, שאלה הטיפולים הקונבנציונליים, והשיטה של נזעי חשמל. ועכשיו יש לנו עוד דרך - ובגלל זה המחקר הזה הוא מעניין".
על רקע הדברים, ובחזרה לממצאים שעלו במחקר, רוזיצקי מדגיש כי לצד הפוטנציאל הגדול, הדרך ליישום קליני רחב עדיין ארוכה. "המחקר עצמו הוא רק התחלתי", הוא אומר, "אבל הוא כן הראה ממצא של הדמיה שהוא אופייני ומאבחן להפרעה נפשית. עשרות נבדקים זו עדיין כמות מוגבלת, ויש צורך לחזור על המחקר הזה עם כמות גדולה יותר של משתתפים. עם זאת, מאוד יכול להיות שבעוד עשר, חמש-עשרה או עשרים שנה נוכל לבצע בדיקות PET-CT למטופלים ולאבחן דיכאון באופן מדויק יותר, אפילו לצפות איזה מטופלים יגיבו טוב יותר לתרופות מסוימות ולהבדיל בין דיכאון לבין פוסט-טראומה. זה נשמע אולי דמיוני", הוא מסכם, "אבל המחקר הזה הוא פורץ דרך בכך שהוא מראה לנו כיוון חדש לאבחון ולטיפול בעתיד".
הבהרה: קטמין הוא חומר מפוקח המוגדר כסם מסוכן בישראל. שימוש בו לטיפול בדיכאון נעשה אך ורק במסגרת רפואית מבוקרת, בפיקוח רופא מוסמך ובמינונים מדודים. הכתבה מתארת ניסוי בהליך מבוקר. שימוש עצמי בקטמין מסוכן ואסור על פי חוק