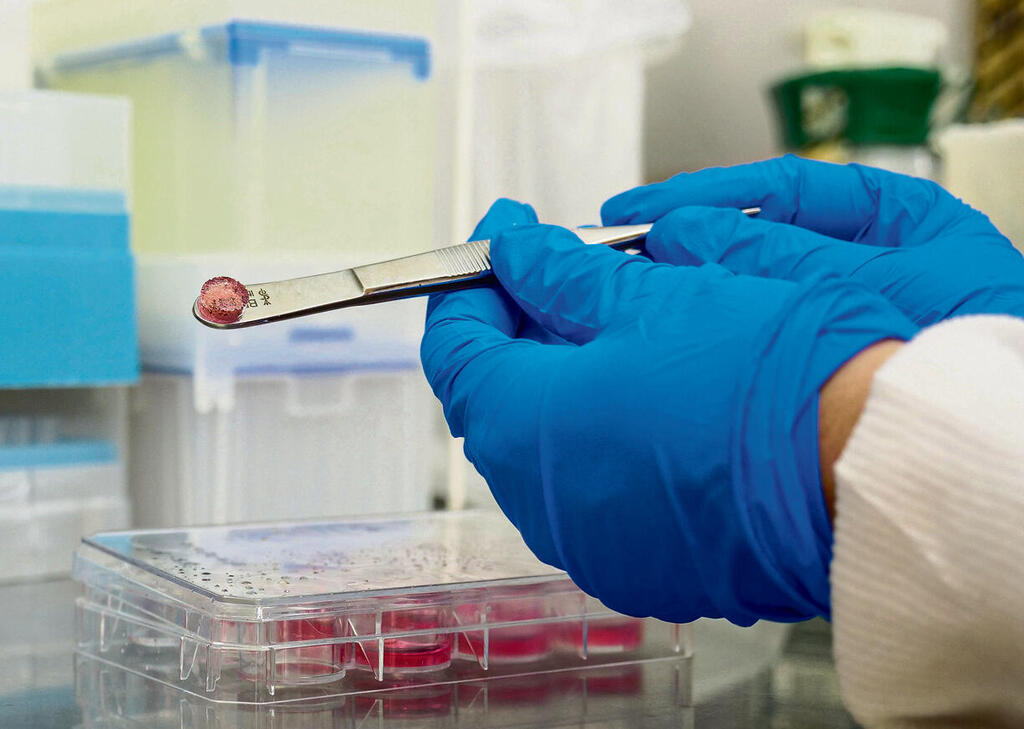
במעבדה בבית החולים רמב"ם, הרחק מחדרי הניתוח ומחלקות האשפוז, מוצבת מכונה. במבט ראשון היא אמנם נראית כמו מדפסת תלת-ממד רגילה, לא משהו שונה בנוף המוכר של שנת 2026, אך בחינה מעמיקה יותר תגלה את האמת המרתקת: במקום דיו או פלסטיק, ראשי המדפסת מלאים בחומרים ביולוגיים ובתאים חיים. שכבה אחר שכבה, היא בונה מבנה זעיר שמדמה, תאמינו או לא - ריאה אנושית.
חלום רפואי גדול
"זה מדהים. עור נחשב כבר לחדשות של אתמול, ריאה זה הדבר החדש", מכריזה ד"ר ארבל ארצי-שנירמן, ראש המרכז לטכנולוגיות ליישום רפואי בקריה הרפואית רמב"ם ומי שמובילה את המחקר. "אני מאוד אוהבת ריאות. אתה צריך לראות את זה. יש לנו עכשיו באינקובטור כלי קטן שבתוכו יש רקמה של ריאה שהיא פונקציונלית - תאים המפרישים ליחה ותאים המכילים מבנים דמויי שיערה שתפקידם לפנות את הלכלוך והחיידקים מהאוויר - ממש כמו בריאה האנושית. ניתן לראות את תזוזת השיערות תחת המיקרוסקופ. אבל זה רק חלק של הריאה. שטח פנים של ריאה שלמה בבן אדם הוא בגודל של מגרש טניס. אין טכנולוגיה היום, למיטב ידיעתי, שיודעת לייצר ריאה שלמה".
היכולת לייצר חלקים מהגוף האנושי במעבדה - זה אולי נשמע כמו רעיון הלקוח מספרי מדע בדיוני מופרעים במיוחד, אך הוא כאן והוא אמיתי, והוא קורה גם בזמן שאתם קוראים את שורות אלו. נכון, זה עדיין לא איבר שלם כמו לב או כליה, אך עבור החוקרים הישראלים מדובר בצעד נוסף לעבר חלום רפואי גדול. במעבדה בקריה הרפואית רמב"ם עושים כיום צעד ראשון ואופטימי בדרך לשם: להדפיס רקמות אנושיות מתאי המטופלים עצמם, ליצור מודלים של מחלות, ולבדוק עליהם תרופות חדשות לפני שהן מגיעות לבני אדם. הפוטנציאל הוא עצום, ולא פחות מכך - גם מרתק להפליא.
מי שמובילה את המחקר, היא כאמור ד"ר ארצי-שנירמן. במעבדה שלה מנסים החוקרים לפרק את הגוף האנושי לשכבות הבסיסיות ביותר - ואז להרכיב אותן מחדש. "להדפיס רקמות זה אומר להבין איך נראית רקמה, איך היא בנויה, אילו תאים יש בתוכה, מה התכונות שלה", היא מסבירה. "משם אנחנו מייצרים במעבדה מבנה גיאומטרי שנאמן לרקמה המקורית ושהרכב התאים שלו גם מתאים. זה מבטיח שהרקמה תהיה פונקציונלית, שאפשר יהיה להשתמש בה ושהיא תדמה את המציאות".
"במקום הטענת דיו שאנחנו מכירים ממדפסת רגילה, אנחנו מטעינים חומר ביולוגי שמרכיב את האיברים השונים שלנו בגוף"
אלא שההבנה הביולוגית היא רק חלק מהסיפור. השלב הבא הוא הניסיון לתרגם את הידע הביולוגי להוראות הדפסה תלת-ממדית. "זה לא כמו מדפסת ביתית, אך הרעיון הוא דומה", היא אומרת. "אם בדף אתה מדפיס בדו-ממד, במדפסת תלת-ממדית מדפיסים בדו-ממד שכבה אחר שכבה לגובה, וכך מתקבל מבנה תלת-ממדי.
"במקום הטענת דיו שאנחנו מכירים ממדפסת רגילה, אנחנו מטעינים חומר ביולוגי שמרכיב את האיברים השונים שלנו בגוף: כדוגמת קולגן, פיברונקטין ולמינין. יש לנו אפשרות להשתמש בחומרים שונים עם הרכב שונה של תאים, ולהדפיס מבנה שמורכב מהשילוב שלהם. בגוף האדם, רקמה לא בנויה מסוג אחד של תאים, ולכן היכולת להדפיס במקביל מספר חומרים ותאים שונים, מאפשרת לנו לייצר מודל עם המורכבות הזאת. אגב, כבר ציינתי שיש לנו את המדפסת הכי טובה שיש?".
איבר מותאם אישית
הייתם סקפטיים? הנה לכם. ואם כל זה נשמע כמו ניסוי מעבדה מסקרן, הרי שהחזון שמאחוריו גדול בהרבה. החוקרים שעובדים על ההדפסות הביולוגיות מדברים כבר שנים על האפשרות שבעתיד ניתן יהיה לייצר רקמות ואפילו איברים שלמים במעבדה - מתאי המטופל עצמו - ובכך לפתור בעיות רפואיות שכיום אין להן מענה אמיתי. תארו לכם עולם שבו רופא כבר לא צריך להמתין לתרומת איבר נדירה או להתפלל שיימצא תורם מתאים בזמן. במקום רשימות המתנה אינסופיות, בתי החולים יחזיקו למעשה במאגר כמעט בלתי מוגבל של איברים להשתלה - רקמות ואיברים שנוצרו במעבדה, מתאי המטופל עצמו, המוכנים לשימוש כשהגוף זקוק להם. בעתיד כל זה יהיה אפשרי.
"כיום יש חוסר גדול באיברים להשתלה. אנשים ממתינים שנים להשתלות", אומרת ד"ר ארצי-שנירמן. "בעתיד באופן תיאורטי נוכל להשתמש בתאים שנלקחו ממטופל ולהדפיס לו איבר שמותאם לו באופן אישי, ללא דחייה חיסונית. זה יהיה דבר אדיר. ניתן יהיה גם להחליף חלקים מאיבר - לייצר השלמה לאיבר שנפגע. לדוגמה, אדם שקיבל התקף לב ורקמת הלב שלו הפכה לצלקתית, ניתן יהיה לשחזר את האזור על ידי הדפסה של רקמה רלוונטית. כנ"ל לגבי כוויות או פציעות בעור - ניתן יהיה להשלים אותן מתאים שבאים מאותו בן אדם. גם עצמות ארוכות. כיום רוב המשתלים הם מטיטניום - חומר מאוד קשיח, כבד. בעתיד אנחנו מקווים שאפשר יהיה להשתמש בחומרים שהם הרבה יותר מותאמים ומדמים עצם".
לדבר הזה יש גם משמעות מקומית. בטח במדינה כמו ישראל שבה בתי החולים מתמודדים בשנים האחרונות עם גל גדול של פצועים מהמערכה האחרונה. פציעות מורכבות של רקמות, כוויות ופגיעות איברים הן אתגר רפואי יומיומי, ולעיתים קרובות הרפואה נאלצת להסתפק בפתרונות שאינם אידיאליים. "אם נוכל להציע לפצועים ולכלל האוכלוסייה פתרונות טובים יותר, זה דבר מבורך ונצרך. יש צורך אמיתי שקיים היום. יש המון התפשרות, והדפסת רקמות יכולה לפתוח פתח לפתרונות הרבה יותר טובים", מוסיפה ד"ר ארצי-שנירמן.
אלא שהעתיד הזה עדיין רחוק. בינתיים, השימושים המעשיים של הדפסה ביולוגית נמצאים במקום אחר, באחד התחומים המאתגרים והיקרים ביותר בעולם הרפואה: פיתוח תרופות חדשות. "אחת הבעיות הגדולות בפיתוח תרופות היא רעילותן. מפתחים תרופה שפותרת בעיה מסוימת וכשנותנים אותה למטופל מגלים שהיא רעילה לכבד או ללב. אין כרגע דרך פשוטה לבדוק את זה. ההדפסה הביולוגית מאפשרת לייצר מודל אנושי שמאפשר לבדוק עליו את התרופות. כך למשל נוכל לקחת תרופה ולבדוק אותה במודל של כבד או לב, ולגלות רעילות – דבר שכבר התחילו לעשות. מדובר במהפכה של ממש, זה משהו שבפירוש אנחנו כבר מפצחים".
מעבר להבטחה הרפואית, ההדפסה הביולוגית נוגעת גם בשאלה מוסרית שמלווה את עולם המדע כבר שנים: השימוש בבעלי חיים בניסויים רפואיים. מודלים אנושיים מודפסים עשויים בעתיד לצמצם באופן משמעותי את הצורך בניסויים כאלה. "זה לא ייתר את הצורך בניסויים בבעלי חיים, אבל זה יקטין אותו משמעותית", מדגישה ד"ר ארצי-שנירמן. "באופן אישי אני מאמינה שצריך להימנע עד כמה שניתן, אבל לצערי זה אף פעם לא יחליף. לפני שמנסים תרופה לראשונה על בני אדם, סביר להניח שהיא תיבדק על חיות. יחד עם זאת, שימוש במודל, יוריד משמעותית את הצורך בניסויים בבעלי חיים".
בדיקת שומות סרטניות
אלא שלמרות ההתקדמות המרשימה, הדרך להדפסת איברים שלמים עדיין רצופה מכשולים. המדע יודע כבר לא מעט על מבנה הרקמות בגוף, אבל לשחזר את המורכבות הזו במדפסת ולהפוך אותה לחלק מתפקד בתוך גוף חי - זה כבר סיפור אחר לגמרי.
"קודם כל, בשביל לייצר איברים שלמים צריך להבין בצורה מדויקת איך האיבר נראה, גם מבחינת הגיאומטריה, האנטומיה, וגם מבחינת הרכב התאים. במקרה הזה אנחנו כבר במצב טוב, אך הטכנולוגיה צריכה להיות מסוגלת להדפיס את אותו מבנה גיאומטרי. אנחנו מתקרבים וזה משתפר. גם החומרים שאנחנו מדפיסים איתם הם אתגר בפני עצמו שמשתפר עם הזמן. אחד האתגרים הגדולים למשל הם כלי הדם. כשאתה מדפיס רקמה אתה צריך שהיא תעבור אינטגרציה לממשק עם הגוף, שנוטריינטים וחמצן יגיעו לרקמה. בגוף יש לנו כלי דם בסמיכות לכל תא, ופה יש אתגר שעדיין לא פתור עד הסוף. אבל גם לאתגר זה אנו מוצאים פתרונות שיילכו וישתפרו, כדי לייצר בתוך הרקמה המודפסת את כלי הדם המאפשר הגעה של ה'אוכל' והחמצן לתאים".
"בעתיד באופן תיאורטי נוכל להשתמש בתאים שנלקחו ממטופל ולהדפיס לו איבר שמותאם לו באופן אישי, ללא דחייה חיסונית"
אבל אם יש דבר אחד שהשיחה עם ד"ר ארבל ארצי-שנירמן ברמב"ם מבהירה מיד, הוא שהעתיד הזה לא מתחיל ביום שבו יודפס לב שלם להשתלה. הוא מתחיל בצעדים קטנים בהרבה. כבר כיום גדלות במעבדה רקמות אנושיות מודפסות שמאפשרות לחוקרים להתבונן מקרוב בתהליכים שמתרחשים בגוף. אלה עדיין לא איברים שלמים, אבל עבור החוקרים מדובר בצעד משמעותי בדרך לשם.
"אנחנו מדפיסים רקמת עור במסגרת שיתוף פעולה עם מחלקת עור בבית החולים", היא מפרטת, "לחלק מהאנשים יש מאות שומות על הגוף ואין היום שום דרך לדעת האם שומה מסוימת תהפוך לסרטנית או לא. אז מה עושים? כל תקופה מצלמים את השומות ועוקבים אחריהן. כדי לשפר את התהליך, אנחנו מדפיסים רקמה בריאה של עור ומתכננים להשתיל בה תאים מנגעים בעור של מטופל כדי לנסות לעקוב ולראות האם שומות מסויימות הופכות לסרטניות או לא. למה זה כל כך מעניין? המודל זמין לנו, אנחנו יכולים לראות את ההתפתחות ואת התהליך במעבדה. אנחנו יכולים לאפיין את כל השלבים, ובמידה ומשהו הופך לסרטני אנחנו יכולים לראות תגובה לתרופות שונות".
ומה מכאן? קשה לדעת מתי בדיוק תגיע נקודת המפנה. האם זה יהיה בעוד עשר שנים, עשרים או אולי אפילו מוקדם יותר. אבל עבור החוקרים שעומדים ליד המדפסות הביולוגיות במעבדות כמו זו שברמב"ם, הכיוון כבר ברור. הדפסת המודלים משמשת למחקרים פורצי דרך, בחינת תרופות וטיפולים, ולמרות שמדובר עדיין בפיסות קטנות של רקמה בתוך אינקובטור, כמו לא מעט פריצות דרך במדע, גם זו הזו מתחילה במשהו שנראה קטן להפליא. כך נולדות מהפכות.