בחודש ינואר האחרון חתמה טבע על הסכם של עד חצי מיליארד דולר עם חברת ההשקעות Royalty Pharma מתוך מטרה להאיץ את פיתוחו של נוגדן חדש למחלות אוטואימוניות - תחום שבו הפער בין הצורך הרפואי לפתרונות הקיימים עדיין משמעותי. במסגרת ההסכם תקבל טבע מימון ראשוני של עשרות מיליוני דולרים לקידום ניסויים קליניים מתקדמים, עם אפשרות להרחבת ההשקעה למאות מיליונים נוספים בהמשך הדרך, בהתאם לתוצאות המחקר.
על פניו, מדובר בעוד מהלך אסטרטגי בעולם הפארמה – כזה שמטרתו לחזק את צנרת הפיתוח ולהבטיח מנועי צמיחה עתידיים בשוק בשווי מיליארדים. אבל מאחורי ההשקעה הזו מסתתרת שאיפה רחבה בהרבה, עם משמעות שעשויה להיות עמוקה בהרבה מתרופה אחת נוספת בשוק. מדובר בניסיון לשנות את נקודת ההתערבות במחלות אוטואימוניות – מקצה התהליך, שבו מטפלים בנזק, אל תחילתו, במקום שבו הוא נוצר. כעת, מאחורי הקלעים של הפיתוח הזה, ענבל בן אליעזר, דיירקטור ומנהלת צוות במחלקה הפרה-קלינית בטבע, מספקת הצצה למקום שבו כל זה קורה - בתוך המעבדות שבהן מדע בסיסי הופך בהדרגה לתקווה טיפולית.
במרכז ההשקעה עומד בשלבי פיתוח הנוגדן TEV-53408, תרופה ניסיונית שנבחנת כיום בשתי חזיתות: צליאק – מחלה כרונית של המעי, וויטיליגו – מחלת עור אוטואימונית עם מענה טיפולי מוגבל. השילוב הזה אינו מקרי: בשני המקרים מדובר במחלות שבהן מערכת החיסון יוצאת משליטה, והתקווה היא שמנגנון משותף יוכל להוות מפתח לשתיהן. שינוי כזה יכול להגדיר מחדש את אופן הטיפול: לא עוד ניהול של המחלה, אלא ניסיון להשפיע על מהלכה.
"הכול מתחיל במחלקת Discovery. הם גילו חלבון שנמצא על תאי מערכת החיסון, שבמצבים של חדירה של גוף זר לגוף, אחראי לסמן את האירוע וליצור דלקת מקומית שתטפל בו. כשהחלבון הזה מבוטא בצורה לא מבוקרת, הוא יכול להיות מניע למחלת הצליאק. הם יצרו נוגדן שהוא בעצם התרופה שלנו, שאמורה לחסום את אותו חלבון"
"צליאק היא מחלה אוטואימונית שפוגעת בתאי המעי", מסבירה בן-אליעזר. "אנשים שחולים בצליאק 'רגישים' לגלוטן - חלבון החיטה. כשהם אוכלים גלוטן, תאים של מערכת החיסון שנמצאים במעי יוצאים מכלל שליטה והורסים את דופן המעי בצורה לא מבוקרת, ונגרמת דלקת כרונית. כתוצאה מכך אנשים שסובלים מהמחלה חווים סימפטומים של כאבים, התכווצויות, נפיחויות, שלשולים, בחילות. נגרמת גם פגיעה בספיגה של המזון ולכן הם גם יכולים, בסופו של דבר, לסבול מאנמיה וחוסרים תזונתיים נוספים".
כיום, בניגוד למחלות אוטואימוניות אחרות שבהן פותחו טיפולים ממוקדים יותר, אפשרויות הטיפול בצליאק נותרו מוגבלות יחסית. "ה'טיפול' היחיד הוא בעצם לא לאכול גלוטן, שהוא בעצם הדרייב המניע של המחלה הזאת", ממשיכה בן-אליעזר. "אם חולי צליאק נמנעים מגלוטן לרוב הם מרגישים בסדר, ואני אומרת לרוב כי לא תמיד זה עובד. יש אנשים שלמרות ההימנעות מגלוטן עדיין מרגישים את התסמינים שתיארתי. עד היום עדיין אין תרופות מלבד ההימנעות".
8 צפייה בגלריה


האחריות לבדוק איך התרופה עובדת נמצאת על הכתפיים שלה. ענבל בן-אליעזר
(צילום: באדיבות טבע)
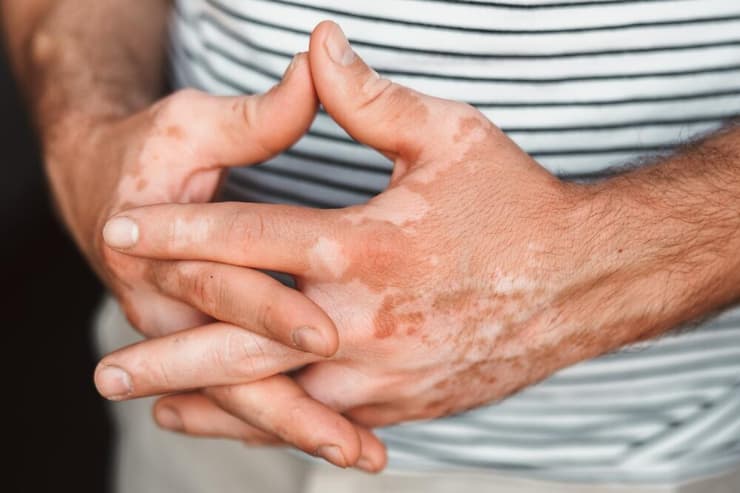
אותה תגובה חיסונית שיוצאת משליטה במעי יכולה להופיע גם באיברים אחרים - וללבוש צורה שונה לגמרי, כמו במחלת הוויטיליגו למשל. "זה מאוד דומה למנגנון של צליאק. יש תאי זיכרון של מערכת החיסון, שיושבים בעור, וגם הם יוצאים מכלל שליטה. רק שבמקרה הזה הם תוקפים את המלנוציטים על העור שלנו – תאים שאחראים לייצור המלנין, הפיגמנט בעור. ברגע שתאי מערכת החיסון פוגעים או הורסים את המלנוציטים, נוצרים כתמים לבנים, שהם סימן ההיכר של המחלה. זה מה שקורה לאנשים עם ויטיליגו. זו מחלה שמאופיינת בכתמים לבנים, הרבה פעמים על הפנים או על כפות הידיים, באזורים שרואים אותם".
אלא שבמקרה של ויטיליגו, ההשלכות אינן רק ביולוגיות. "זו לא מחלה שמשפיעה בריאותית בשום צורה, אבל היא משפיעה מאוד מבחינה נפשית", מדגישה בן-אליעזר. "אנשים בציבור מסתכלים על אנשים שסובלים מוויטיליגו כאילו הם מידבקים. הם מנסים להתרחק מהם ושואלים המון שאלות. זה פוגע ממש בהערכה העצמית ובבריאות הנפשית של האנשים האלה. בגלל זה המחלה מקושרת הרבה לדיכאון וחוסר יציאה מהבית. העול הנפשי משמעותי, ומהווה את הבעיה העיקרית".
הדרך הארוכה מתיאוריה לתרופה
עד לא מזמן, הטיפול במחלות אוטואימוניות התבסס במידה רבה על גישה גסה יחסית: דיכוי רחב של מערכת החיסון, בתקווה לצמצם את הנזק. אלא שבשנים האחרונות הולכת ומתבססת גישה אחרת, מדויקת וזהירה יותר, שמבקשת להבין את המנגנון לפני שמנסים לעצור אותו. תרופות ביולוגיות שמכוונות לחלבונים או למסלולים ספציפיים, כמו התרופה הנוכחית שמפותחת בימים אלו בטבע, הן התוצאה הישירה של השינוי הזה.
"בניגוד למולקולות קטנות שהן פחות ספציפיות, ולכן יכולות לגרום ליותר תופעות לוואי, התרופות הביולוגיות, בגלל שהן מאוד ספציפיות, גורמות להרבה פחות תופעות לוואי", מסבירה בן-אליעזר. "הן גם נשארות הרבה יותר זמן בגוף. אפשר לקחת אותן פעם בכמה שבועות. בשנים האחרונות התרופות האלה נכנסו לשוק בצורה מאוד חזקה. יש היום קו פיתוח מאוד חזק בכל העולם לפתח תרופות ביולוגיות. זה ממש הכיוון שאנחנו רואים כרגע".

אבל גם אחרי שנמצאת מולקולה מבטיחה, הדרך ממעבדה לטיפול שמגיע לחולים עוד רחוקה. זהו שלב שבו הפיתוח מתרחב - לא רק כדי לבדוק אם התרופה עובדת, אלא גם איך, באילו תנאים ומהו המחיר של ההתערבות. במילים אחרות: זהו הרגע שבו המדע נדרש להוכיח את עצמו מחוץ לתיאוריה. כדי להפוך מנגנון חיסוני למטרה טיפולית, לא מספיק להבין אותו - צריך גם לבדוק אם אפשר לגעת בו מבלי לשבש את המערכת כולה. כאן נכנס שלב הפיתוח, שבו כל היפותזה נבחנת בפועל: איך הגוף מגיב, מה מחיר ההתערבות, ואם יש כאן פוטנציאל אמיתי או כיוון שלא יבשיל. כך למעשה נולדת כל תרופה.
"האתגר הוא להבין את מנגנון הפעולה של התרופה. להבין אם היא משפיעה על עוד תאים, אילו מנגנונים אפשר לפצח למחלות אחרות. מה קורה לתא ברגע שהתרופה נקשרת אליו: האם היא מורידה את הפעילות שלו, האם היא מורידה את הרמה שלו, האם היא מונעת קשירה שלו לתא אחר שאמור לבצע פעולה אחרת?"
"הכול מתחיל במחלקת Discovery אצלנו בטבע. זהו השלב הראשון של גילוי ופיתוח התרופה. המחלקה הזאת יושבת באוסטרליה, והם פיתחו לראשונה את התרופה שאנחנו עובדים עליה במטרה לטפל בצליאק", אומרת בן-אליעזר. "על ידי קריאה של ספרות מחקרית ומאמרים הם גילו שיש חלבון מסוים שנמצא על תאי מערכת החיסון, שבמצבים רגילים, כאשר יש חדירה של גוף זר או פתוגן לגוף, אחראי לסמן את האירוע וליצור דלקת מקומית שתטפל בגוף הזר הזה. כשהחלבון הזה מבוטא בצורה לא מבוקרת, למשל במעי, הוא יכול להיות מניע למחלת הצליאק".
ברגע שמנגנון זה התבהר, התחילה העבודה האמיתית. "הם יצרו נוגדן שהוא בעצם התרופה שלנו, שאמורה לחסום את אותו חלבון ובכך להוריד את רמות הדלקת ואת כמות תאי מערכת החיסון והפעילות שלהם. כך הם הראו היתכנות ראשונית לטיפול במחלת הצליאק. ברגע שתרופה עוברת את השלב הראשוני של ההיתכנות של Discovery, היא עוברת לשלב השני - השלב הקדם-קליני", מסבירה בן-אליעזר.
עבורה, השלב הזה מתרחש בנתניה - באתר המחקר והפיתוח של טבע, אחד המרכזים הבולטים של החברה. המתחם, ששורשיו בשנות ה-60 ונרכש על ידי טבע ב-1988, משתרע על פני יותר מ-9,000 מ"ר של מעבדות, ובו פועלים למעלה מ-400 חוקרים המעורבים בפיתוח תרופות למגוון מחלות - מהפרעות נוירולוגיות ועד מחלות אוטואימוניות כמו ויטיליגו.
"בשלב שלנו אנחנו מקבלים תרופה שיש לה איזשהם סימנים של יעילות מסוימת, ואנחנו מכינים אותה להיכנס לשלבים הקליניים לבדיקות בבני אדם. באמצעות מחקר מדעי אנחנו מנסים להבין איך היא עובדת, אם יש בה סיכונים, ובעצם איך להביא אותה לשלבים קליניים".
יש אתגרים בדרך?
"האתגר הוא להבין את מנגנון הפעולה של התרופה, כלומר מה היא עושה. אנחנו מכוונים אותה לטפל בסוג תא מסוים, אז חשוב להבין אם היא משפיעה על עוד תאים, אילו מנגנונים אפשר לפצח למחלות אחרות עם אותה תרופה. האתגרים הביולוגיים שלנו הם לנסות להבין איך התרופה נקשרת לחלבון, ומה קורה לתא ברגע שהתרופה נקשרת אליו: האם היא מורידה את הפעילות או הרמה שלו, האם היא מונעת קשירה שלו לתא אחר שאמור לבצע פעולה אחרת או מונעת שחרור של חומר מאותו תא? המטרה היא להבין מה בדיוק היא עושה לתא שאותו אנחנו מנסים לטרגט כדי לטפל במחלה, ואז איך זה משפיע על המחלה. אלה הן בעצם השאלות המרכזיות שעומדות לנגד עינינו כשאנחנו מנסים לפתח תרופה למחלה מסוימת".
בנוסף, השלב הקדם-קליני עוסק גם בהרחבת האפשרויות. "כשהתרופה מגיעה אלינו, אנחנו מסתכלים ושואלים את עצמנו, לפי הביולוגיה שידועה מהספרות, מה עוד אפשר לעשות כדי להגיע לכמה שיותר מחלות וחולים ברחבי העולם - ומה שישר קפץ לנו בהקשר של TEV-53408 זאת מחלת הוויטיליגו", אומרת בן-אליעזר.
"במחלה, כאמור, החלבון המדובר מבוטא ביתר בעור ומשפיע על תאי מערכת החיסון. עשינו ניסויים במעבדה, הראינו שניתן גם לטפל במחלה הזאת בעזרת התרופה והכנו חבילה פרה-קלינית לקראת בדיקה בשלבים קליניים יותר. כיום התרופה נמצאת בשלבים קליניים גם למחלת הצליאק וגם למחלת הוויטיליגו. במסגרת הזאת חשוב לי לציין את הצוותים בפרה-קליניקה. יש לנו צוותים של אנשים מאוד חזקים, מדענים שמגיעים מהאוניברסיטאות הכי טובות בארץ ובעולם, עם ניסיון מאוד רחב, שרואים לנגד עיניהם רק את המדע ואיך ניתן לפצח את השאלות המאוד מורכבות האלה שדיברנו עליהן. זה מרגיש שאנחנו עובדים ממש בחזית המדע".
מהמעבדה לבני אדם
בנקודה הזו הפיתוח עובר משלב של שליטה יחסית ותנאים מבוקרים לשלב שבו הוא נמצא כעת - השלב הקליני. הניסויים הקליניים נועדו לא רק לאשר את מה שכבר נצפה במעבדה, אלא גם לחשוף את מה שלא ניתן היה לראות קודם: תגובות שונות בין אנשים, תופעות לוואי בלתי צפויות והגבולות האמיתיים של ההתערבות.

"יש שלושה שלבים: פאזה ראשונה, שנייה ושלישית", מסבירה בן אליעזר. "בכל שלב בודקים את התרופה על אנשים, ובכל פעם מגדילים את מספר המשתתפים כדי להוכיח בטיחות וגם יעילות של התרופה. כרגע אנחנו בשלבים הקליניים, ויש לנו צוות בארץ שתומך בפעילות יחד עם צוות בארה"ב. גם ניהול הפרויקט יושב בישראל, מי שמסתכלים על כל הפרויקט ועל כל הזוויות שלו. כל היחידות השונות בטבע - הייצור, הפרה-קליניקה, הקליניקה והצוותים שמתפעלים את הניסויים הקליניים וגם השיווק - כולם צריכים לעבוד בהרמוניה כדי שהתרופה תתקדם בקצב הנכון ותגיע לחולים כמה שיותר מהר. ברגע שיסתיימו השלבים הקליניים ויתקבל אישור מה-FDA, התרופה תגיע לשוק".
אבל במקביל למציאת המנגנון ולבדיקת ההיתכנות הקלינית, יש עוד שלב קריטי בדרך: להפוך את הרעיון לתהליך שניתן לייצר. זהו מעבר מעולם המחקר לעולם ההנדסה – שבו כבר לא שואלים רק אם התרופה עובדת, אלא אם אפשר לייצר אותה בצורה עקבית, מדויקת ובכמויות שיאפשרו להביא אותה לחולים.
"תהליך הייצור של תרופות ביולוגיות קורה בתאים, בניגוד למולקולות קטנות שניתן לייצר בצורה כימית במעבדה. התרופות הביולוגיות נוצרות על ידי תאים, ויש לנו יחידות שלמות בטבע שזה מה שהן עושות - מנסות לייצר תהליך כמה שיותר מדויק, סטרילי ונכון עבור כל תרופה בנפרד", מתארת בן-אליעזר. "יש לנו יחידה כזו בישראל וגם יחידה כזו בארה"ב, שזה מה שהן עושות: מפתחות את השיטה והתהליך לייצר את התרופה".
איך זה קורה בפועל?
"מייצרים תאים שמבטאים את הנוגדן, את התרופה, ובעצם משחררים אותו לנוזל שבו הם נמצאים. גם צריך לייצר את התא שמייצר את החלבון, כלומר את הנוגדן שלנו, וגם לייצר את התהליך שבו ממצים את התרופה מהנוזל. עושים את זה בהתחלה בסקייל קטן. משם לאט-לאט מגדילים את הסקייל כדי שנוכל לייצר כמויות גדולות לשימוש בתרופה בניסויים הקליניים, וגם אחר כך ברגע שזה מגיע לשוק".
האם כבר יש צפי?
"שאלה מצוינת. אנחנו בשלבים קליניים כרגע, ואנחנו מתקדמים שלב-שלב. המטרה היא להגיע בשנים הקרובות לשוק, אבל מוקדם להגיד מתי".
בעתיד נוכל לרפא עוד מחלות?
"בהחלט. זה הכיוון שלנו כרגע. בצורה פרה-קלינית בודקים את התרופה למחלות אוטואימוניות נוספות, ומקווים שנוכל להביא את התרופה לבדיקה באנשים בשלבים קליניים גם בהן. זה בהחלט העתיד שלנו, אך עוד מוקדם להגיד".